標本作製の手引き

顕微鏡下でヒトの細胞や組織を調べる理由はたくさんあります。医学・生物学の研究は、細胞や組織の正常な構造と機能、および、それらが構成する臓器や構造に関する知識によって支えられています。正常な健康状態では、細胞および他の組織成分は、規則的で認識可能なパターンで配置されています。
幅広い化学的および物理的影響によって引き起こされる変化は、顕微鏡レベルでの構造変化に反映され、多くの疾患は、正常な状態とは異なる典型的な構造的および化学的異常によって特徴付けられます。これらの変化を同定して特定の疾患に関連付けることは、組織病理学と細胞病理学の基礎であり、現代医学の重要な専門分野です。
顕微鏡検査は、血液学(血液の研究)、微生物学(寄生虫やウイルスを含む微生物の研究)、さらに広い生物学の領域である、動物学や植物学の分野で重要な役割を果たしています。これらすべての分野で、標本は顕微鏡で検査されます。
顕微鏡
顕微鏡 にはさまざまな形式がありますが、最も一般的に使用されるのは「明視野」顕微鏡です。この顕微鏡では、(電子顕微鏡のような電子ビームとは対照的に)試料を通過する光線で標本に光を当てます。明視野顕微鏡を使用してうまく観察するための、標本に関する一般的な要件は次のとおりです:
- 標本内の細胞やその他の成分が「生きているような」状態で保存されていること(このプロセスは「固定」と呼ばれます)
- 標本が不透明ではなく透明であり、光が通過できること
- 標本が薄く平らで、単細胞層しか存在しないこと
- 一部の構成要素に異なる色を付け(染色)、明確に区別できるようになっていること
作製のオプション
顕微鏡検査の要件のため、標本作製のオプションは以下のものに制限されています:
- ホールマウント:生体全体や構造全体が、顕微鏡スライドに直接のせることができるほど十分に小さいか薄い場合(例:小さな単細胞生物や多細胞生物、またはスライド上に薄く伸ばすことができる膜など)
- 「押しつぶし」標本:中身を明らかにするために細胞がスライド上に意図的に押しつぶします(例:細胞が破壊されて染色体が明らかになった植物標本)
- 塗抹標本:標本は液体(血液、精液、脳脊髄液、微生物の培養液など)に懸濁された細胞からなっているか、個々の細胞が臓器の表面または内部からかきとられたり、吸引されたりします(剥離細胞診)。塗抹標本は、女性の子宮頸がんをスクリーニングとしてよく知られている「Pap(パパニコロウ)検査」の基礎です。
- 切片:標本が何らかの方法で保持されているため、非常に薄いスライスとして薄切することができ、そのスライスをスライドにのせ、染色することができます。切片は、「ミクロトーム」と呼ばれる機器を使用して作製します。
これらのオプションのうち、ホールマウントと切片のみが、個々の細胞と細胞外構成要素間の構造的関係を保持します。塗抹標本と押しつぶし標本の作製は、個々の細胞と相対的な細胞数についての詳細を提供しますが、構造的な関係は失われます。切片の作製は、これらの方法の中で最も技術的に複雑で、特殊な機器とかなりの専門知識が必要です。病理医による切片の顕微鏡検査は、がん診断の基礎になっています。動物と植物いずれの材料でも、切片を作成する方法論は似ていますが、以下の説明は動物(ヒト)の組織に関するものです。
切片の作製
大部分の新鮮な組織は、非常にデリケートで、簡単に変形させられたり、損傷を受けるので、薄切する際に何らかの方法で支えられない限り、薄い切片(スライス)を作製することは不可能です。通常、標本は切片を作製する前に保存、すなわち「固定」する必要があります。大きく分けて、2つの方法があります。
1. 組織を急速に凍結し、 クリオスタットミクロトーム (冷凍チャンバー内のミクロトーム)で凍結したまま切片を作製します。凍結切片は極めて迅速に作製できるため、外科手術の手引きのために術中診断が必要な場合や、(一部の組織化学的検査において)細胞の化学的構成に対する何らかの干渉を回避する必要がある場合に使用されます。
2. 後に適切な物理的性質を有する固体に変換することができる液剤を標本に浸透させ、薄い切片を作製することができるようにすることができます。エポキシ樹脂やメタクリレート樹脂など、さまざまな試薬が標本の浸透およびサポートに使用できますが、通常の光学顕微鏡検査では、パラフィンワックスベースの組織学的検査用ワックスが最も一般的です。この方法がいわゆる「パラフィン切片」です。これらの切片は通常、「回転式」ミクロトームで作製されます。「回転」は、機器の切断動作を説明しています。すべての組織病理学検査室で、パラフィン切片はほぼすべての標本から日常的に作製され、診断に使用されています。
以下の段落で、パラフィン切片を作製する際の主なステップについて説明します。何百もの標本が毎日処理される大規模な専門の組織病理学検査室のレイアウトとワークフローが、これらのステップにより、大まかに規定されます。


検体の受領
組織学的検査のために受領する検体は、さまざまなソースから来る可能性があります。その範囲は、非常に大きな標本や臓器全体から組織の小さな断片に至ります。たとえば、以下に示すものが組織病理学検査室で一般的に受け取る標本タイプの一部です。
- 切除標本(外科的生検):手術時に臓器全体や患部が切除されます
- 切開生検標本:診断のために患部内から組織が採取されます
- パンチ生検:疑わしい組織の小片を検査するためにパンチを使って採取されます(皮膚からが多い)
- 薄片生検:組織の小さな薄片を表面から薄く削りとられます(通常は皮膚)
- キュレット:子宮内膜や子宮頸部から小さな組織片が採取されます
- コア生検:特別な針を使用し、時に皮膚を通して(経皮的に)少量の組織サンプルが取り出されます。
標本は通常、固定液(保存剤)に入った状態で受け取りますが、時々採取したばかりのものが到着することがあり、その場合直ちに固定する必要があります。標本を検査室に受け入れる前に、識別(ラベル付け)と付属文書を慎重にチェックし、すべての詳細が記録され、「標本の追跡」が開始されます。患者または研究標本を適切に識別し、不正確さのリスクを最小限に抑えることが重要です。
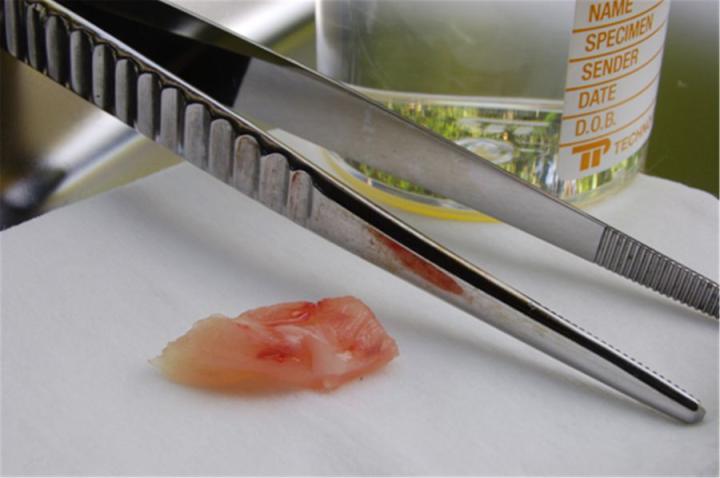
固定
固定は、顕微鏡検査用の標本を作製する上で、重要なステップです。その目的は、腐敗を防ぎ、細胞や組織を「生きているような」状態に保つことです。そのために、固定が行うことは、酵素活性を止め、微生物を殺し、標本を硬化させることです。この間も、分子構造は十分に保たれるので、適切な染色法(抗原抗体反応をともなうものやDNA・RNAの保存に依存するものなど)を適用することが可能になります。血液供給から検体を分離した後、固定開始が早いほど、良い結果が得られます。最も使用されることの多い固定液は ホルムアルデヒドで、通常は、リン酸緩衝液の形態です(「ホルマリン」と呼ばれることが多い)。理想的には、検体を処理する前に6〜12時間ホルマリンに浸して固定する必要があります。

目視検査
目視検査。「カットアップ」と呼ばれることが多い目視検査は、外観、小片の数、大きさなど、検体の慎重な検査と説明を伴います。大きな検体では、適切な領域から代表的な小片を作成するために、さらに切り分けることが必要になる場合があります。例えば、腫瘍が完全に除去されたことを保証するために、腫瘍の切除縁から複数のサンプルが採取される場合があります。小さな標本の場合は、標本全体を処理することができます。処理用に選択された組織は、カセット(小さな穴あきバスケット)に入れられ、複数のバッチが組織プロセッサにロードされ、ワックス処理まで実施されます。
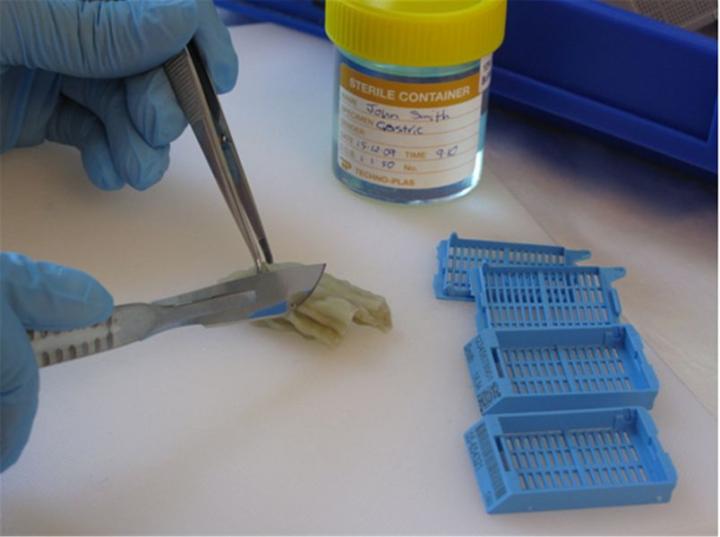
プロセッシング
パラフィン切片を作製するために、大きなバッチの 標本を処理する 場合は、 「ティッシュプロセッサー」 と呼ばれる自動機器が用いられます。これらの機器は、標本に一連のさまざまな溶媒を浸透させることができ、最後に標本は溶融パラフィンワックス内に入れられます。標本は最初、水溶性ですが(水ベース)、次に脱水溶媒と置換溶媒(通常はエタノールとキシレン)に標本を複数回のステップを経て通過させる必要があり、最後に標本は溶融ワックス(疎水性で水と混和しない)に入れられます。標本の特定のバッチに対して選択された「処理スケジュール」の時間とステップの詳細は、標本の性質とサイズによって異なります。スケジュールは、小さな標本の場合は最短1時間、大きな標本の場合は12時間以上です。多くの検査室では、処理の大部分は一晩で行われます。現在、ワークフローを改善し、所用時間を短縮するため迅速な処理が可能なプロセッサを検査室で使用するように、かなりのプレッシャーかかっています。

包埋
処理後、標本は 包埋センター に置かれ、そこでカセットから取り出され、ワックスで満たされたモールドに入れられます。この段階で標本の向きを注意深く調整します。これにより、切片が切断される平面が決定され、最終的に顕微鏡下で異常な領域が見えるかどうかが決定される可能性があるためです。組織が処理されたカセットには標本識別の詳細が記載されており、モールドの上に配置され、さらにワックスを追加することにより取り付けられます。標本「ブロック」を冷却表面で固化させ、セットする際にモールドを取り外します。ワックスで満たされ、ブロックの一部を形成しているカセットは、ミクロトーム内に固定するための安定したベースを提供します。これで、標本を含むブロックを切片にする準備が整いました。

セクショニング
切片は「ミクロトーム」と呼ばれる精密機器で、非常に鋭い鋼の刃を使って薄切されます。パラフィン切片は通常3〜5 µmの厚さで薄切し、単層の細胞のみが切片を構成するようにします(赤血球の直径は約7 µmです)。包埋剤としてのパラフィンワックスの利点の1つは、切片が薄切されたときに端と端がくっつき、切片の「リボン」が形成されることです。これにより、取り扱いが簡単になります。
切片はフローテーションバス中の温水の表面に「浮かべ」平らになります。これをすくい上げ、顕微鏡のスライドに載せます。完全に乾燥した後、染色可能になります。


染色
メラニンなどのいくつかの天然色素を除いて、ほとんどの標本を構成する細胞やその他の成分は無色です。明視野顕微鏡を使用して構造の詳細を明らかにするためには、何らかの形の染色が必要です。重要な構造情報を提供する際の出発点として広く使用されている通常の染色は ヘマトキシリン・エオシン(HE)染色です。この方法では、細胞核は青色に染色され、細胞質および多くの細胞外成分はピンクの色合いになります。組織病理学では、HE染色のみで多くの疾患を診断できます。ただし、完全な鑑別診断を提供するために追加情報が必要になる場合があり、これにはさらに専門的な染色技術が必要です。これらは、特定の構造または微生物を定義するために色素または金属含浸を使用する「特殊染色」か、または、標識抗体を用いて診断に役立つタンパク質の位置を明らかにする 免疫組織化学法(IHC)である可能性があります。。特定のDNAまたはRNA配列を検出するには、 in-situ ハイブリダイゼーション(ISH)などの分子的手法が必要になる場合もあります。これらの方法はすべてパラフィン切片に適用でき、ほとんどの場合、作成されたスライドは完全に安定しており、何年も保存できます。
染色後、切片はガラス製のカバーグラスで覆われ、病理医に送られます。病理医は、これらを顕微鏡で観察し、適切な診断を下し、レポートを作成します。

About the presenter

Geoffrey Rolls is a Histology Consultant with decades of experience in the field. He is a former Senior Lecturer in histopathology in the Department of Laboratory Medicine, RMIT University in Melbourne, Australia.
Related Content
Leica Biosystems Knowledge Pathway content is subject to the Leica Biosystems website terms of use, available at: Legal Notice. The content, including webinars, training presentations and related materials is intended to provide general information regarding particular subjects of interest to health care professionals and is not intended to be, and should not be construed as, medical, regulatory or legal advice. The views and opinions expressed in any third-party content reflect the personal views and opinions of the speaker(s)/author(s) and do not necessarily represent or reflect the views or opinions of Leica Biosystems, its employees or agents. Any links contained in the content which provides access to third party resources or content is provided for convenience only.
For the use of any product, the applicable product documentation, including information guides, inserts and operation manuals should be consulted.
Copyright © 2026 Leica Biosystems division of Leica Microsystems, Inc. and its Leica Biosystems affiliates. All rights reserved. LEICA and the Leica Logo are registered trademarks of Leica Microsystems IR GmbH.