Eine Einführung in die Entkalkung

Als Entkalkung oder Demineralisierung werden Techniken zur Entfernung von Mineralien aus Knochen oder anderem kalkhaltigem Gewebe beschrieben. Sie sind Voraussetzung dafür, dass anschließend hochwertige Paraffinschnitte angefertigt werden können, und sollen den Erhalt der mikroskopischen Gewebestrukturen garantieren. Die Entkalkung wird durchgeführt, nachdem die Probe gründlich fixiert wurde und bevor sie mit Paraffin infiltriert wird. In diesem Artikel wird die grundlegende Struktur des Knochens beschrieben und es werden methodische Alternativen zur Vorbereitung von Knochenschnitten aufgezeigt. Verschiedene Verfahren zur Entkalkung und Möglichkeiten zur Überwachung des Prozesses werden diskutiert und es werden die Formulierungen der meistverwendeten Reagenzien angegeben.
Einleitung
Der Histologe hat mehrere Möglichkeiten, wenn es darum geht, Knochenschnitte oder Präparate aus anderen kalkhaltigen Proben zu erstellen. Bei der Auswahl einer Technik zur Probenvorbereitung und - infiltration muss berücksichtigt werden, welche weiteren Untersuchungen vorgesehen sind. Wenn beispielsweise eine metabolische Knochenerkrankung untersucht wird und mineralisierter Knochen von Osteoid unterschieden werden soll oder wenn morphometrische Messungen erforderlich sind, kann es notwendig sein, die Mineralien im Gewebe zu erhalten und Schnitte aus nicht entkalkten Proben anzufertigen. Die Härte mineralisierten Knochens schränkt die Techniken, die zur Schnitterstellung angewandt werden können, stark ein. Nach der Fixierung können Knochenproben direkt in dünne Scheiben gesägt und dann abgeschliffen werden, um sogenannte Knochenschliffe zu erzeugen (Abbildung 1). Es ist auch möglich, Knochenproben mit Acryl- oder Epoxidharzen zu infiltrieren, die nach der Polymerisation eine Härte aufweisen, die der von mineralisiertem Knochen entspricht. Aus den so infiltrierten Proben können Knochenschliffe hergestellt und sogar Mikrotomschnitte angefertigt werden, wenn ein Hartschnittmikrotom zur Verfügung steht, z. B. das Leica SM2500. Außerdem wird ein Wolframcarbid- oder Diamantmesser benötigt (Abbildung 2). Gefrierschnitte aus mineralisierter Spongiosa können ebenfalls erzeugt werden.1-3
Viel häufiger werden Knochen und andere kalkhaltige Proben nach der Fixierung entkalkt (demineralisiert) und nach einer Standardmethode weiterverarbeitet, um Paraffinschnitte anzufertigen. Entkalkte Schnitte erlauben eine Untersuchung des Knochenmarks und erleichtern die Diagnose von Tumoren, Infektionen und anderen Zuständen. Es können ganz unterschiedliche Probentypen anfallen, darunter trepanierter Darmbeinkamm, chirurgische Resektate wie zum Beispiel ein Oberschenkelkopf, aber auch aus Amputaten entnommene Gewebe. Oft werden hochauflösende Röntgenaufnahmen genutzt, um die geeignetsten Knochenproben für die weitere Verarbeitung zu identifizieren. Aber kalkhaltige Gewebe sind mehr als Knochen: Auch im Zuge von degenerativen Prozessen kann es zur Verkalkung kommen, etwa bei einer Nekrose (mit dystrophischer Verkalkung). Auch die Wände von Blutgefäßen, die Nieren, die Lunge und andere Gewebsstrukturen können verkalken. Da es sich hierbei um Verkalkungen von vitalem Gewebe handelt, spricht man von metastatischer Verkalkung.4 Eine ausgedehnte Verkalkung kann die Schnitterstellung wesentlich behindern oder gar unmöglich machen, wenn die Probe zunächst nicht entkalkt wird. Eine spontane Lösung dieses Problems bietet die sogenannte „Oberflächenentkalkung“, bei der die Schnittfläche des bereits angefertigten Paraffinblocks entkalkt wird. Auf diese Technik wird vor allem dann zurückgegriffen, wenn unerwartet Verkalkungen auftreten und die Schnitterstellung behindern.
Die Entkalkung ist ein relativ einfaches Verfahren und wird in Standardtexten der histologischen Technik ausführlich diskutiert.1-3 Um jedoch qualitativ hochwertige Ergebnisse zu erzielen, sind einige Punkte zu beachten.
Struktur des Knochens
Knochen besteht aus Zellen, sogenannten Osteozyten, die von mineralisierter Matrix umgeben sind, die Kollagenfasern vom Typ I enthält. In der Matrix liegt Kalzium in Form von Hydroxyapatitkristallen [Ca10(PO4)6(OH)2] vor, die sich zwischen den Faserelementen ablagern. Während der Entkalkung lösen sich diese Kristalle. Wenn der Prozess korrekt durchgeführt wird, bleibt die Gewebekohäsion erhalten und die entkalkte Probe weist die physikalischen Eigenschaften eines dichten fibrösen Bindegewebes auf.
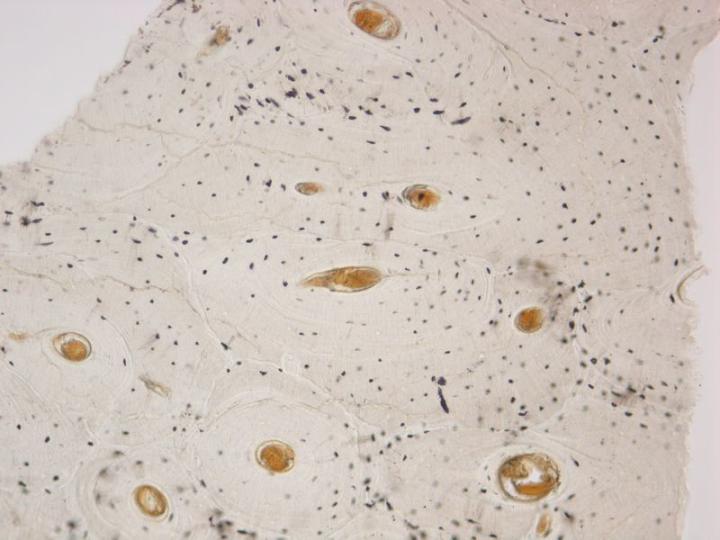
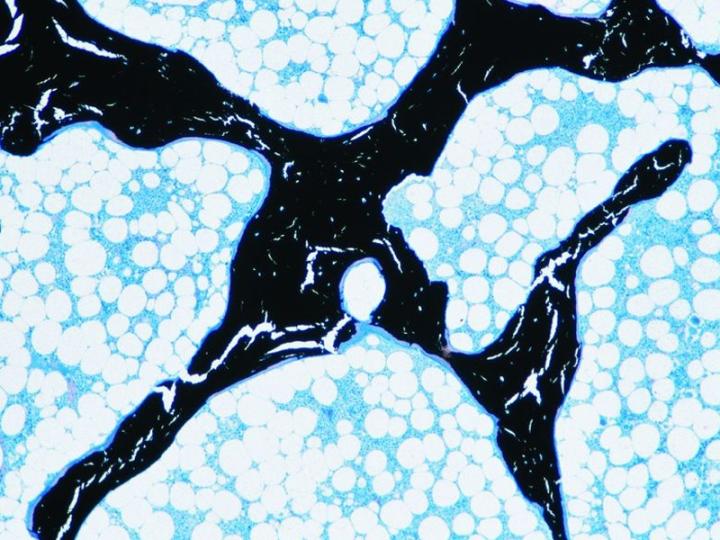
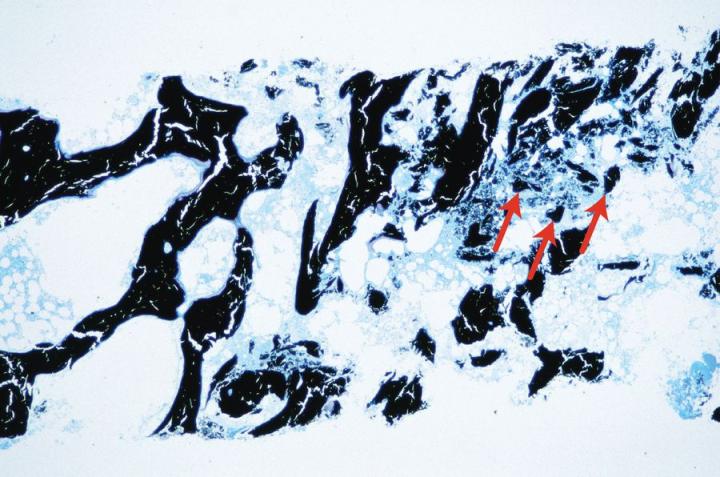
Morphologisch lassen sich zwei Arten von reifen Knochen unterscheiden. Die Kortikalis, auch kompakter Knochen genannt, bildet die Schäfte der Röhrenknochen und den Großteil der platten Knochen des Schädels. Sie charakterisiert sich durch eine sehr dichte Struktur, die auf einer definierten Anordnung von zylindrischen Strukturen basiert, die Osteone genannt werden (Abbildung 3). Im Gegensatz dazu ist die Spongiosa, die auch als Schwammknochen bezeichnet wird, viel feiner gegliedert. Sie besteht aus dünnen Bälkchen, sogenannten Trabeculae, die zahlreiche kleine Räume begrenzen, in denen sich das Knochenmark befindet. Spongiosa findet sich im Inneren der Wirbel und der Epiphysen der Röhrenknochen (Abbildung 4). Beide Arten von Knochen entwickeln sich in Schichten, wobei sich Lamellen bilden, in denen die Kollagenfasern so ausgerichtet sind, dass die Funktion des jeweiligen Knochens bestmöglich erfüllt werden kann. Im polarisierten Licht ergibt sich daraus ein charakteristisches Bild (Abbildung 5).2-3, 5
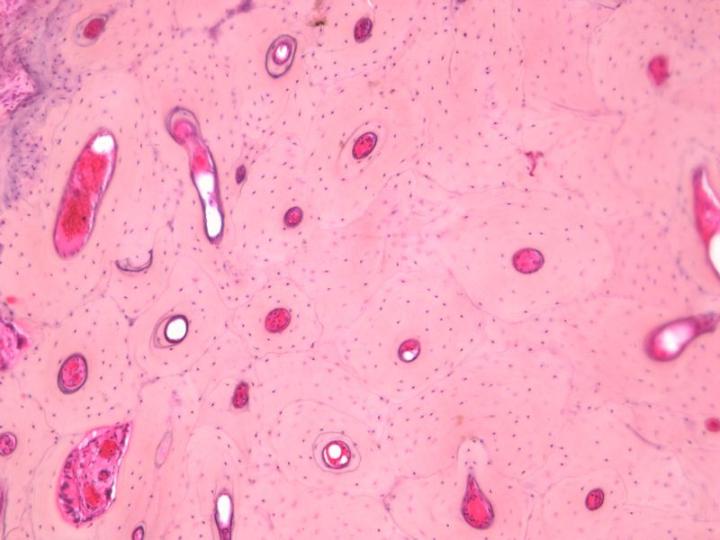
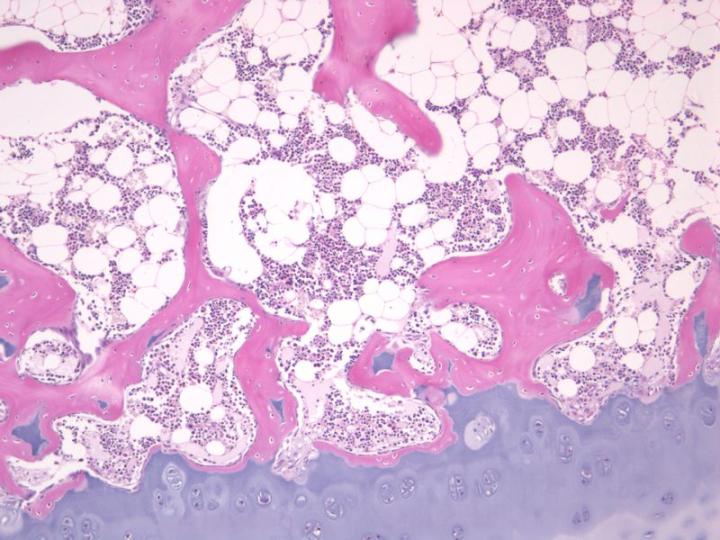

Es ist wichtig, zu berücksichtigen, welche Art Knochenprobe verarbeitet werden soll, da die relativen Anteile an kortikalem und spongiösem Knochen einen entscheidenden Einfluss auf die notwendige Entkalkungs- und Infiltrationszeit haben. Trepanierter Darmbeinkamm zum Beispiel besteht aus einem Kortikalisrand, der einen Zylinder aus Spongiosa begrenzt. Während der Entkalkung sind es die Mineralsalze aus diesem Kortikalisrand, die am längsten Widerstand leisten und sich als letzte lösen. Um anschließend gute Schnitte erstellen zu können, ist eine vollständige Entkalkung dieses Randes aber unbedingt nötig.
Fixierung von Knochenproben
Um die zellulären und faserigen Elemente des Knochens vor säureinduzierten Schäden zu schützen, müssen diese Proben vor der Entkalkung unbedingt gründlich fixiert werden.2-3 Unzureichend fixierte Proben weichen während der Entkalkung auf und lassen sich nur schlecht färben. In Bereichen mit Knochenmark fällt das besonders auf. Daher ist es üblich, für Knochenproben längere Fixierungszeiten zu wählen, bevor mit der Entkalkung begonnen wird. Um das Eindringen des Fixiermittels in den Knochen zu erleichtern, sollten umgebende Haut und Weichgewebe soweit möglich entfernt werden. Knochenproben sollten so früh wie möglich in dünne Scheiben gesägt werden, um die Fixierung zu verbessern, und es sollte stets ein ausreichendes Volumen an Fixiermittel zur Verfügung stehen. Zur Präparation der Knochenscheiben eignen sich hochwertige feine Zahnsägen. Grobe Sägen können erhebliche Schäden verursachen und Knochenfragmente in das in der Probe vorhandene Weichgewebe drängen (siehe Abbildung 6).
Gepuffertes Formalin eignet sich gut zur Fixierung von Knochenproben, aber wenn die Erhaltung des Knochenmarks wichtig ist, werden zum Teil Alternativen wie eines der Zink-Formalin-Fixative, B5, Davidsons Alkohol-Formalin-Eisessig-Fixativ oder Bouin'sche Lösung bevorzugt.
Entkalkungsmittel – Übersicht
Im Wesentlichen gibt es drei Arten von Entkalkungsmitteln:
- auf starken Mineralsäuren basierende Entkalker,
- auf schwächeren organischen Säuren basierende Entkalker
- und Entkalkungsmittel aus Chelatbildnern.
Der Einfachheit wegen wählen die meisten Labore aus den zahlreichen kommerziell erhältlichen Entkalkungsmitteln aus. Potenzielle Anwender dieser Reagenzien sollten das relevante Sicherheitsdatenblatt konsultieren, um die aktiven Komponenten des Produkts zu identifizieren, insofern diese nicht eindeutig auf der äußeren Verpackung angegeben sind.
Entkalkungsmittel – Starke Säuren
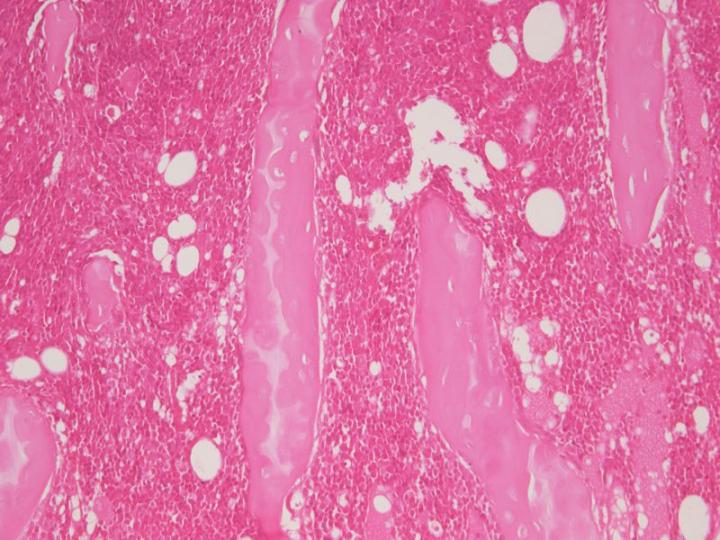
Mineralsäuren wie Salzsäure oder Salpetersäure in Konzentrationen bis zu 10 % entkalken am schnellsten, aber wenn die Proben diesen starken Säuren zu lange ausgesetzt bleiben, kommt es leicht zum Verlust der Kernfärbung und zur Mazeration des Gewebes. Deshalb ist es wichtig, einen geeigneten Endpunkttest durchzuführen und die Exposition der Proben gegenüber diesen Reagenzien zu minimieren. Kommerziell erhältliche Entkalkungsmittel, die als Schnellentkalker beworben werden, basieren in der Regel auf starken Säuren, meistens auf Salzsäure. Sie sollten vorsichtig verwendet werden und es ist unbedingt auf die Anwendungshinweise zu achten, wenn gute Ergebnisse erzielt werden sollen. Das Entkalkungsmittel Surgipath Decalcifier II® beispielsweise wirkt schnell und enthält Salzsäure. Abbildung 7 zeigt die Folgen einer Behandlung mit einer starken Säure, die über den angemessenen Endpunkt hinaus fortgeführt wurde.
In Tabelle 1 sind einige der gängigen Entkalkungsmittel auf Mineralsäurebasis aufgeführt. Umfassendere Aufstellungen finden sich in den entsprechend zu konsultierenden Lehrbüchern der Histotechnologie.
Tabelle 1: Entkalkungsmittel auf Basis starker Säuren
|
Entkalker |
Formel |
Bemerkungen |
|
Salpetersäure6 |
5 % in destilliertem Wasser |
wirkt schnell, Endpunktüberschreitung beeinträchtigt Färbeergebnisse |
|
Perenyi'sche Flüssigkeit6 (1882) |
40 ml Salpetersäure 10 % 30 ml Chromsäure 0,5 % 30 ml Ethanol absolut |
ein traditionelles Entkalkungsmittel, das langsamer entkalkt als verdünnte Salpetersäure; wirkt immer noch schnell und eine Endpunktüberschreitung beeinträchtigt auch hier die Färbeergebnisse |
|
Salzsäure3 |
5-10 % in destilliertem Wasser |
Formalin sollte ausgewaschen werden, bevor die Probe in Salzsäure gelegt wird, um die Bildung von karzinogenem Bischlormethylether zu vermeiden; wirkt schnell, Endpunktüberschreitung beeinträchtigt Färbeergebnisse |
|
Ebner‘sche Flüssigkeit6 |
50 ml gesättigte NaCl-Lösung 42 ml destilliertes Wasser 8 ml HCl |
wirkt schnell, Endpunktüberschreitung beeinträchtigt Färbeergebnisse |
Entkalkungsmittel – Schwache Säuren
Schwache Säuren wie Ameisensäure sind beliebt und werden häufig zur Entkalkung verwendet. 10%ige Ameisensäure kann als einfache wässrige Lösung oder in Kombination mit Formalin oder einem Puffer verwendet werden. Obwohl sie langsamer wirkt als die starken Säuren, ermöglicht sie eine gewebeschonende Entkalkung, die nur selten Probleme mit der Kernfärbung macht.1, 7 Ein Beispiel für ein kommerziell erhältliches Entkalkungsmittel, das auf Ameisensäure basiert, ist Surgipath Decalcifier I®. Neben der Ameisensäure enthält dieses Produkt Formalin, das über die schonende Entkalkung hinaus wahrscheinlich zur Fixierung beiträgt. Auch andere schwache Säuren, z. B. Trichloressigsäure (TCA), haben als Entkalkungsmittel Verwendung gefunden. Pikrinsäure, Bestandteil einiger Fixiermittel, wirkt schwach entkalkend.
Tabelle 2: Entkalkungsmittel auf Basis schwacher Säuren
|
Entkalker |
Zusammensetzung |
Bemerkungen |
|
Ameisensäure8 |
10 % in destilliertem Wasser |
Ein einfacher, effektiver Entkalker |
|
Evans und Krajian8 |
25 ml Ameisensäure 10 g Natriumzitrat 75 ml destilliertes Wasser |
wirksamer Entkalker auf Basis von Ameisensäure, zitratgepuffert |
|
Kristensen8 |
18 ml Ameisensäure 3,5 g Natriumformiat 82 ml destilliertes Wasser |
wirksamer Entkalker auf Basis von Ameisensäure, formiatgepuffert |
|
Gooding and Stewart8 |
5-25 ml Ameisensäure 5 ml Formaldehyd 40 % 75 ml destilliertes Wasser |
Entkalker auf Basis von Ameisensäure plus Formalin, dem fixierende und entkalkende Eigenschaften zugeschrieben werden |
Entkalkungsmittel – Chelatbildner
Chelatbildner wie Ethylendiamintetraessigsäure (EDTA) wirken, indem sie die Kalziumionen von der Oberfläche des Apatitkristalls abnehmen und so nach und nach dessen Größe verringern. Da dieser Prozess zwar schonend, aber nur sehr langsam abläuft – je nach Probengröße kann die Entkalkung Wochen dauern – ist dieses Reagens nicht für dringende Proben geeignet. In der Forschung allerdings, wo das Hauptaugenmerk auf dem bestmöglichen Erhalt der Gewebemorphologie liegt oder bestimmte molekulare Elemente für eine Weiterverarbeitung mittels IHC, FISH oder PCR erhalten werden müssen, kann EDTA gut eingesetzt werden.9 Es wird bei einer Konzentration von etwa 14 % in neutraler Lösung verwendet.1,10 Die Geschwindigkeit, mit der EDTA entkalkt, ist pH-abhängig. Wie bereits erwähnt, wird es standardmäßig bei einem pH-Wert von 7,0 eingesetzt. Ein pH-Wert von 10,0 beschleunigt die Entkalkung, aber nicht alle Gewebestrukturen vertragen ein derart alkalisches Milieu.10
Tabelle 3: Chelatbildner
|
Entkalker |
Formel |
Bemerkungen |
|
Neutrale EDTA1 |
250 g EDTA-Dinatriumsalz 1750 ml destilliertes Wasser pH-Wert durch Zugabe von NaOH auf 7,0 einstellen (ca. 25 g werden benötigt) |
wirkt langsam, verursacht aber kaum Gewebeschäden; Standardfärbungen werden kaum beeinträchtigt |
Faktoren, die die Entkalkungsgeschwindigkeit beeinflussen
Konzentration
Die Konzentration des Wirkstoffs beeinflusst die Geschwindigkeit, mit der Kalzium aus der Probe herausgelöst wird. In der Literatur zu findende Formulierungen für Entkalkungsmittel streben nach einem Gleichgewicht zwischen Schnelligkeit und gewebeschonender Behandlung. Es muss daran gedacht werden, dass die Wirkstoffkonzentration über die Zeit abnimmt, da der Wirkstoff Kalzium bindet und so verbraucht wird. Daher ist es ratsam, ein ausreichend großes Volumen an Entkalkungsmitteln bereitzustellen und es während des Entkalkungsvorgangs mehrmals zu wechseln.
Temperatur
Auch im Hinblick auf die Temperatur gilt es, einen Mittelweg zu finden: Hohe Temperaturen beschleunigen die Entkalkung, gehen aber mit einer stärkeren Gewebeschädigung einher.
Probenbewegung
Eine sanfte Probenbewegung auf dem Schüttler kann die Entkalkung leicht beschleunigen.1
Gewebezugänglichkeit
Wie bei der Fixierung sollte auch bei der Entkalkung darauf geachtet werden, dass sämtliche Oberflächen der Probe von der Flüssigkeit umspült werden und somit gut erreichbar sind. Das erleichtert die Diffusion, das Eindringen des Entkalkungsmittels in die Probe und damit die Lösung und Entfernung von Kalzium.
Andere Techniken für eine effizientere Entkalkung
Die Kombination von EDTA und Ultraschall hilft, die Entkalkung von Gewebeproben zu beschleunigen, die unter Einsatz einer Trepanfräse entnommen werden und zur Molekularanalyse vorgesehen sind. Während des Prozesses muss die Temperatur sorgfältig kontrolliert werden.9 Man hat auch versucht, die Salzsäure-basierte Entkalkung durch eine gleichzeitige Mikrowellenbehandlung zu fördern, aber die hohen Temperaturen können die Gewebemorphologie verändern und Färbeartefakte verursachen.10 Ionenaustauschharze wurden ebenfalls in einige Entkalkungsprotokolle aufgenommen. Sie werden dem Behälter mit Entkalkungsmittel zugefügt und fangen das ionisierte Kalzium ab, sodass die Wirksamkeit der Säure länger erhalten bleibt. Wenn Entkalker auf Säurebasis in ausreichenden Volumina verwendet und regelmäßig ersetzt werden, ist der Einsatz solcher Harze wahrscheinlich unnötig.3 Bei der elektrolytischen Entkalkung wird der Knochen in einen Entkalker auf Säurebasis gelegt, es werden Elektroden angeschlossen und eine Spannung angelegt. Aufgrund der potenziellen Erhitzung der Probe mit subsequenten Wärmeschäden hat diese Technik allerdings keine breite Akzeptanz gefunden.3
Bestimmung des Endpunkts der Entkalkung
Wenn hochqualitative Ergebnisse erzielt werden sollen, ist es wichtig, den genauen Zeitpunkt zu erfassen, an dem das gesamte Kalzium herausgelöst wurde, da der weitere Verbleib der Probe im Entkalkungsmittel mit zunehmenden Gewebeschäden verbunden ist. Eine übermäßige Entkalkung, insbesondere auf Basis starker Säuren, verdirbt die Färbung von basophilen Elementen wie Zellkernen und kann unter bestimmten Umständen zur Mazeration der weicheren Gewebeelemente führen. Andererseits können Proben, die unvollständig entkalkt sind, schwierig oder gar unmöglich zu schneiden sein.
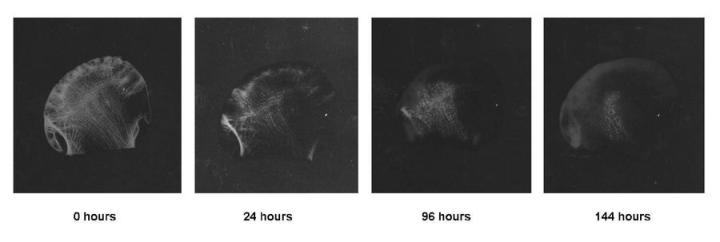
Die beste Methode zur Bestimmung des optimalen Endzeitpunkts, insbesondere bei großen Proben wie Femurköpfen, ist das Röntgen. Eine gute Röntgenaufnahme lässt auch winzige Kalziumreste erkennen und steht einer weiteren Entkalkung, wenn nötig, nicht im Wege. Das Röntgen der Probe eignet sich hervorragend zur Nachverfolgung des Entkalkungsprozesses, insbesondere bei großen Proben wie den bereits benannten Femurköpfen (Abbildung 8). Bei Verwendung bestimmter Entkalker auf Säurebasis, vor allem Ameisensäure, kann außerdem ein einfacher chemischer Test angewendet werden. Hier wird die entkalkende Lösung getestet, nicht das Gewebe selbst. Eine kleine Menge der zuletzt genutzten Entkalkungslösung wird mit Ammoniumhydroxid neutralisiert und anschließend mit Ammoniumoxalatlösung versetzt.1Befindet sich Kalzium in der Lösung, fällt Kalziumoxalat aus – der Test liefert ein positives Ergebnis und zeigt an, dass die Entkalkung noch unvollständig ist und nach wie vor Kalzium aus der Probe gelöst wird. Verständlicherweise ist für diesen Test Entkalkungslösung zu nutzen, die kürzlich gewechselt wurde und vielleicht seit einer Stunde auf die Probe wirkt. Physikalische Tests erfordern eine mechanische Manipulation der Probe, die gebogen, sondiert oder getrimmt werden muss, um verbleibende Kalkherde zu „fühlen“. Während sich erfahrene Techniker durchaus als feinfühlig genug erweisen können, gelten diese Methoden im Allgemeinen als unzuverlässig. Aber es können nicht nur Kalziumablagerungen übersehen werden, auch die Probe kann beim Biegen oder Untersuchen Schaden nehmen.7 Darüber hinaus wurde eine Methode zur Bestimmung des Endpunkts der Entkalkung beschrieben, bei dem die Probe zunächst gespült und anschließend sorgfältig gewogen wird. Aufgrund der deutlicheren Gewichtsabnahme eignet sich diese Technik eher für große Proben.10
Wenn Sie glauben, dass der Entkalkungsendpunkt kurz bevorsteht und Sie den Prozess verlangsamen möchten, um eine übermäßige Entkalkung und daraus resultierende Gewebeschäden zu vermeiden, können Sie die Probe aus dem Entkalkungsmittel nehmen, spülen und wieder in Formalin legen. Letzteres ist besonders wichtig, wenn mit Salzsäure entkalkt wird. Die Entkalkung kann dann zu einem beliebigen passenderen Zeitpunkt fortgeführt werden.10 Auch eine Kühlung der Probe in ihrem Entkalker auf 4 °C verlangsamt den Prozess.1

Behandlung nach der Entkalkung und vor der Infiltration
Es sind verschiedene Methoden zur Beseitigung von Säureresten beschrieben. Sie können durch gründliches Waschen in Leitungswasser entfernt oder durch die Anwendung alkalischer Lösungen neutralisiert werden. Im Allgemeinen sollte ein kurzes, effektives Waschen in Leitungswasser ausreichen, weil eventuell persistierende Säurereste dann spätestens bei der Infiltration entfernt werden.1 Es ist trotzdem wichtig, so viel Entkalkungsmittel wie möglich auszuwaschen, um eine Kontamination der Reagenzien zu vermeiden, die in den Folgeschritten Anwendung finden.
Auswahl eines geeigneten Zeitplans für entkalkten Knochen und andere entkalkte Gewebe
Nach der Demineralisierung kann die weitere Verarbeitung nach Standardprotokollen erfolgen. Man beachte, dass Knochenproben auch nach vollständiger Entkalkung noch dichte Bereiche enthalten, die eine gründliche Infiltration erfordern. Das gilt besonders für die Kortikalis. Es ist besser, einem Protokoll zu folgen, das etwas länger ist, und nicht zu kurz zu greifen. Welches Protokoll sich empfiehlt, hängt von der Art und Größe der Proben ab. Die Qualität der fertigen Blöcke lässt sich in der Regel verbessern, wenn die Wachsinfiltration vakuumgestützt wird.
Oberflächenentkalkung
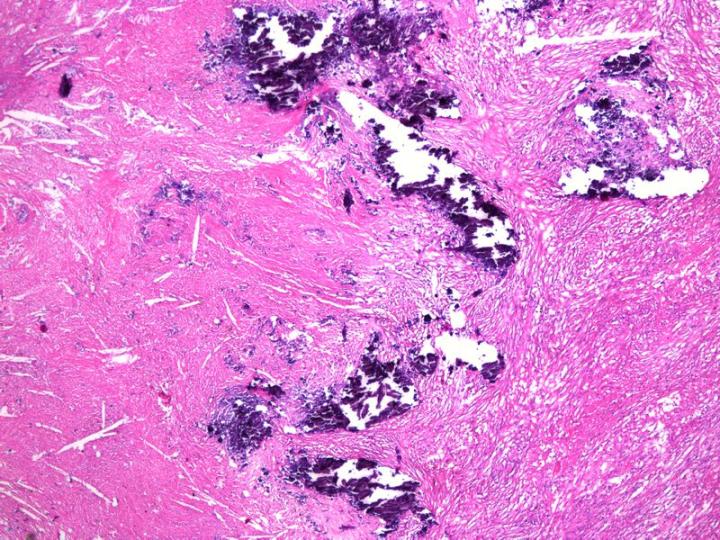
Hierbei handelt es sich um eine Methode zur Lösung kleinerer Kalziumablagerungen, wie sie zuweilen unerwartet in Paraffinblöcken auftreten (Abbildung 10). Solche Ablagerungen werden in der Regel erst beim Trimmen entdeckt, manchmal auch noch später. Dann gilt es, ein angemessenes Gleichgewicht zu finden, das eine Entkalkung ermöglicht, aber die Oberfläche des Blocks nicht zerstört. Nach der Freilegung des Gewebes kann der Block aus dem Mikrotom genommen und für 15-60 Minuten mit der schnittrelevanten Seite nach unten in ein Entkalkungsmittel auf Säurebasis gelegt werden. So kann der Entkalker in die oberflächlichen Gewebeschichten eindringen und das störende Kalzium lösen. Anschließend sollte der Block zur Entfernung von Säureresten gründlich in Wasser gespült werden. Nach erneuter Kühlung steht er wieder zur Schnitterstellung bereit. Eine sorgfältige Neuausrichtung des Blocks ist erforderlich, weil bei dieser Notlösung lediglich ein geringer Anteil des Gewebes entkalkt wird, sodass nur ein paar Schnitte angefertigt werden können.1, 11
Fazit
Die Entkalkung ist ein unkomplizierter Prozess, aber für gute Ergebnisse bedarf es:
- einer sorgfältigen Vorbeurteilung der Probe
- einer gründlichen Fixierung
- der Anfertigung von Gewebescheiben einer Dicke, die Fixierung und Infiltration erleichtert
- der Wahl eines geeigneten Entkalkungsmittels in ausreichender Menge, das zudem regelmäßig gewechselt wird
- der exakten Bestimmung des Endpunkts der Entkalkung
- einer gründlichen Infiltration über einen angemessenen Zeitraum
About the presenter

Geoffrey Rolls is a Histology Consultant with decades of experience in the field. He is a former Senior Lecturer in histopathology in the Department of Laboratory Medicine, RMIT University in Melbourne, Australia.
Referenzen
- Page KM. Bone. In Bancroft JD and Stevens A eds. Theory and Practice of Histological Techniques. New York: Churchill Livingstone, 1996.
- Moore RJ. Bone. In Woods AE und Ellis RC eds. Laboratory histopathology. New York: Churchill Livingstone, 1994;7.2-10.
- Carson FL. Histotechnology. 2nd ed. Chicago: ASCP Press, 2007.
- Vardaxis NJ. Pathology for the health sciences. Melbourne: Macmillan Australia Pty Ltd, 1997.
- Junge B, Heide JW. Wheater's Functional Histology. 4th ed. Edinburgh: Churchill Livingstone, 2000.
- Clayden EC. Practical section cutting and staining. Edinburgh: Churchill Livingstone, 1971.
- Skinner RA, Hickmon SG, Lumpkin CK, Aronson J, Nicholas RW. Decalcified Bone: Twenty Years of Successful Specimen Management. The Journal of Histotechnology 1997;20;267-277.
- Wallington EA. Histological Methods for Bone. London: Butterworths, 1972.
- Reineke T, Jenni B, Abdou MT et al. Ultrasonic Decalcification Offers New Perspectives for Rapid FISH , DNA, and RT_PCR Ananlysis in Bone Marrow Trephines Am J Surgical Pathology 2006;30.
- Callis G, Sterchi D. Decalcification of Bone: Literature Review and Practical Study of Various Decalcifying Agents, Methods, and Their Effects on Bone Histology. The Journal of Histotechnology 1998;21;49-58.
- Rolls GO. Difficult Blocks and Reprocessing. Leica Microsystems, 2011.
Related Content
Die Inhalte des Knowledge Pathway von Leica Biosystems unterliegen den Nutzungsbedingungen der Website von Leica Biosystems, die hier eingesehen werden können: Rechtlicher Hinweis. Der Inhalt, einschließlich der Webinare, Schulungspräsentationen und ähnlicher Materialien, soll allgemeine Informationen zu bestimmten Themen liefern, die für medizinische Fachkräfte von Interesse sind. Er soll explizit nicht der medizinischen, behördlichen oder rechtlichen Beratung dienen und kann diese auch nicht ersetzen. Die Ansichten und Meinungen, die in Inhalten Dritter zum Ausdruck gebracht werden, spiegeln die persönlichen Auffassungen der Sprecher/Autoren wider und decken sich nicht notwendigerweise mit denen von Leica Biosystems, seinen Mitarbeitern oder Vertretern. Jegliche in den Inhalten enthaltene Links, die auf Quellen oder Inhalte Dritter verweisen, werden lediglich aus Gründen Ihrer Annehmlichkeit zur Verfügung gestellt.
Vor dem Gebrauch sollten die Produktinformationen, Beilagen und Bedienungsanleitungen der jeweiligen Medikamente und Geräte konsultiert werden.
Copyright © 2026 Leica Biosystems division of Leica Microsystems, Inc. and its Leica Biosystems affiliates. All rights reserved. LEICA and the Leica Logo are registered trademarks of Leica Microsystems IR GmbH.