Eine Einführung in die Präparation mikroskopischer Proben

Es gibt viele Gründe, menschliche Zellen und Gewebe unter dem Mikroskop anzuschauen. Biologische und medizinische Forschung bauen auf dem Wissen über die normale Struktur und Funktion von Zellen, Geweben, Organen und deren Komponenten auf. Im gesunden, physiologischen Zustand sind sämtliche Gewebeelemente in mehr oder weniger regelmäßigen, wiedererkennbaren Mustern angeordnet. Veränderungen, wie sie durch eine Vielzahl biologischer, chemischer und physikalischer Einflüsse hervorgerufen werden, spiegeln sich in Abweichungen von diesem Normalzustand wider und sind auf mikroskopischer Ebene identifizierbar. Zahlreiche Krankheiten zeichnen sich durch typische Anomalien aus, aus denen sich eine pathologische Diagnose ableiten lässt. Damit werden die Histopathologie und Zytopathologie zu wichtigen Fachbereichen der modernen Medizin. Die Mikroskopie spielt auch eine wichtige Rolle in der Hämatologie, also der Untersuchung von Blut, in der Mikrobiologie, in der man sich mit Mikroorganismen beschäftigt, und im weiteren Sinne in der Biologie, Zoologie und Botanik. In all diesen Disziplinen werden Proben unter dem Mikroskop untersucht.
Mikroskopie
Es gibt viele verschiedene Varianten der Mikroskopie, aber die am häufigsten eingesetzte ist die sogenannte Hellfeldmikroskopie, in der die Probe von Lichtstrahlen durchdrungen und so beleuchtet wird. Im Gegensatz dazu werden Proben in der Elektronenmikroskopie von einem Elektronenstrahl passiert. Die allgemeinen Anforderungen an eine Probe, die in der Hellfeldmikroskopie untersucht werden soll, sind:
- Erhalt von Zellen und andere Gewebeelemente in einem „lebensähnlichen“ Zustand, was im Rahmen der Fixierung erreicht wird
- Transparenz und Lichtdurchlässigkeit der Probe
- Dünne und Flachheit, sodass die Probe nur eine einzige Zellschicht umfasst
- Anfärbung verschiedener Gewebekomponenten in unterschiedlichen Farbtönen, was sie deutlich unterscheidbar macht
Möglichkeiten zur Probenpräparation
Aufgrund dieser Anforderungen an mikroskopische Präparate beschränken sich die Möglichkeiten zur Probenpräparation auf:
- Ganzpräparate, wie sie für Organismen oder Strukturen angefertigt werden können, die klein und dünn genug sind, um direkt auf einen Objektträger platziert zu werden (z. B. ein einzelliger oder kleiner vielzelliger Organismus oder eine Membran, die flach und dünn ausgebreitet werden kann)
- Quetschpräparate, bei denen die Zellen absichtlich auf einem Objektträger zerdrückt werden, um ihren Inhalt untersuchen zu können, z. B. Quetschungen pflanzlicher Proben zur Beurteilung der Chromosomen
- Abstriche von Proben, in denen die Zellen in einer Flüssigkeit suspendiert sind (z. B. Blut, Liquor, Sperma oder eine Mikroorganismenkultur), oder bei denen einzelne Zellen von einer Oberfläche oder aus dem Inneren eines Organs abgeschabt, abgebürstet oder aspiriert wurden (Exfoliativzytologie); beim bekannten Pap-Abstrich werden Zellen von der Schleimhaut des Gebärmutterhalses gewonnen und im Rahmen der Krebsvorsorge untersucht
- Schnitte, wobei nach einer entsprechenden Stabilisierung des Gewebes sehr dünne Scheiben geschnitten, auf Objektträger aufgezogen und gefärbt werden; die Schnitterstellung erfolgt in einem als „Mikrotom“ bezeichneten Gerät
Nur in Ganzpräparaten und Schnitten bleiben die strukturellen Beziehungen zwischen einzelnen Zellen und extrazellulären Gewebebestandteilen erhalten. Die Erstellung von Schnitten ist die technisch anspruchsvollste Methode, erfordert neben speziellen Geräten auch ein umfassendes Fachwissen. Die mikroskopische Untersuchung von Schnittpräparaten durch einen Pathologen bildet die Grundlage der Krebsdiagnostik. Obwohl sich die Methoden zur Anfertigung von Schnitten aus tierischem und pflanzlichem Material ähneln, sind einige Besonderheiten zu beachten. Die folgende Beschreibung bezieht sich auf tierische einschließlich humaner Gewebe.
Vorbereitung der Schnitterstellung
Frisches Gewebe ist in der Regel sehr empfindlich und leicht zu beschädigen. Deshalb ist es unmöglich, frische Proben in derart dünne Scheiben zu schneiden, wie sie für mikroskopische Untersuchungen gebraucht werden. Das Gewebe muss also gestützt und somit in seiner Struktur gestärkt werden. Außerdem ist eine Konservierung der Probe erforderlich. Sie erfolgt während der sogenannten Fixierung und beugt der Degeneration des Gewebes vor. Im Großen und Ganzen gibt es zwei Strategien, wie diese Ziele erreicht werden können:
1. Das Gewebe kann schockgefroren und im gefrorenen Zustand geschnitten werden. Dazu benötigt man ein Mikrotom mit Gefrierkammer, ein Kryostat. So erzeugte Schnitte werden als „Gefrierschnitte“ bezeichnet. Gefrierschnitte lassen sich sehr schnell anfertigen und werden daher bevorzugt, wenn eine intraoperative Diagnose erforderlich ist, von der der weitere Verlauf eines chirurgischen Eingriffs abhängt. Außerdem hat der Verzicht auf jegliche chemische Behandlung Vorteile, wenn chemische Charakteristika erhalten bleiben sollen, wie es für einige histochemische Untersuchungen notwendig ist.
2. Alternativ können Proben mit einer Flüssigkeit infiltriert werden, die man anschließend erstarren lässt. So werden „Blöcke“ angefertigt, deren physikalische Eigenschaften es ermöglichen, dünne Schnitte zu schneiden. Für diese Infiltration stehen verschiedene Flüssigkeiten zur Verfügung, die dem Gewebe mehr oder weniger starken Halt verleihen. Epoxid- und Methacrylatharze seien als Beispiele genannt, aber histologische Wachse auf Paraffinbasis sind mit Sicherheit die weitverbreitetsten Infiltrationsmittel für die routinemäßige Lichtmikroskopie. Unter Verwendung dieser Wachse werden Paraffinschnitte erstellt und normalerweise erfolgt das mit einem „rotierenden“ Mikrotom. „Rotierend“ bezieht sich auf den Antrieb des Mikrotoms, nicht auf die Bewegung der Klinge, und das Gerät wird Rotationsmikrotom genannt. Paraffinschnitte werden in allen histopathologischen Laboratorien aus fast jeder Probe routinemäßig hergestellt und in der Diagnostik verwendet.
Die folgenden Abschnitte beschreiben die wichtigsten Schritte bei der Vorbereitung von Paraffinschnitten. Es sind eben diese Schritte, die im Allgemeinen die räumliche Gestaltung und den Arbeitsablauf in großen histopathologischen Labors bestimmen, in denen täglich Hunderte von Proben verarbeitet werden.


Probenannahme
Proben, die zur histologischen Untersuchung ins Labor kommen, stammen aus verschiedenen Quellen. Sie unterscheiden sich auch sonst recht stark und reichen von ganzen Organen über großvolumige Exemplare bis hin zu winzigen Gewebefragmenten. Um diese Variabilität zu verdeutlichen, sind im Folgenden einige Probentypen aufgeführt, die üblicherweise in ein histopathologisches Labor gesandt werden:
- Exzisionsproben oder chirurgische Biopsien, für die während eines Eingriffs ganze Organe oder betroffene Bereiche entnommen werden
- Inzisionsbiopsien, bei denen mittels eines Einschnitts ein kleineres Gewebestück aus einem betroffenen Bereich entfernt wird
- Stanzbiopsien, bei denen mit einer Stanze ein kleiner Gewebezylinder gewonnen wird (oft Haut)
- Rasierbiopsien, bei denen Gewebefragmente von einer Oberfläche, in der Regel von der Haut, abrasiert werden
- Kürettage, also jenes Gewebe, das bei der Ausschabung eines Hohlorgans gewonnen wird, wobei es sich meist um Gebärmutterschleimhaut handelt
- Kernbiopsien, die mithilfe einer speziellen Nadel entnommen werden, die zum Teil direkt durch die Haut in das Zielgewebe geführt wird
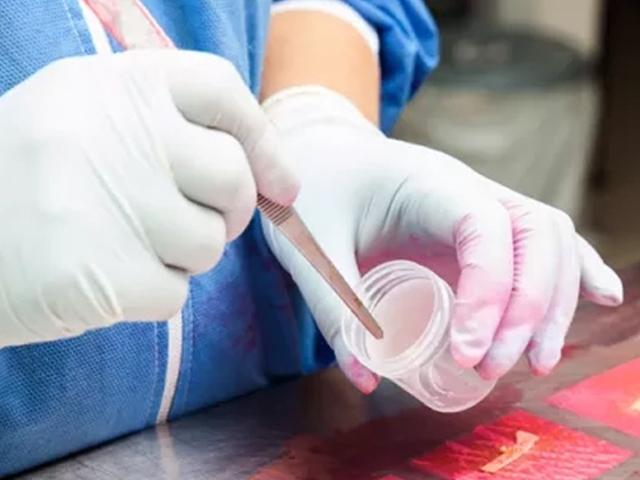
Die meisten Proben werden vor dem Versand in Fixiermittel gelegt, aber auch frisches Material kommt gelegentlich an und muss so schnell wie möglich fixiert werden. Bevor die Probenannahme quittiert wird, sollte unbedingt die Etikettierung und Begleitdokumentation überprüft und ggf. vervollständigt werden, um eine lückenlose Nachverfolgbarkeit garantieren zu können. Es ist wichtig, dass alle Proben, egal ob sie von Patienten oder aus der Forschung stammen, eindeutig identifizierbar sind und das Risiko von Verwechslungen minimiert wird.
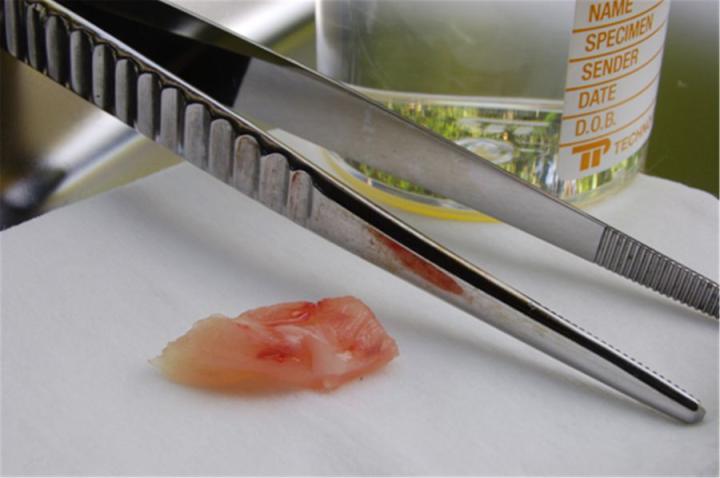
Fixierung
Die Fixierung ist ein entscheidender Schritt bei der Vorbereitung von Proben für die mikroskopische Untersuchung. Das Ziel der Fixierung besteht darin, den Zerfall von Gewebeelementen zu verhindern und Zellen und Gewebe in einem möglichst lebensähnlichen Zustand zu erhalten. Erreicht wird das, indem die Enzymaktivität gestoppt, Mikroorganismen abgetötet und die Probe gehärtet wird, während die molekulare Struktur erhalten bleibt. Letztere ist Voraussetzung für die Bindung bestimmter Farbstoffe und damit für die Anfärbbarkeit des Gewebes mittels verschiedener Methoden, einschließlich solcher, die Antigen-Antikörper-Reaktionen erfordern oder von DNA und RNA abhängen. Je weniger Zeit zwischen der Unterbrechung der Blutversorgung des Gewebes und der Fixierung der Probe vergeht, desto besser. Das gängigste Fixiermittel ist Formaldehyd. Es liegt meist in einer Phosphat-gepufferten Lösung vor, die auch als Formalin bezeichnet wird. Im Idealfall sollten Proben sechs bis zwölf Stunden lang durch Eintauchen in Formalin fixiert werden, bevor sie infiltriert werden.

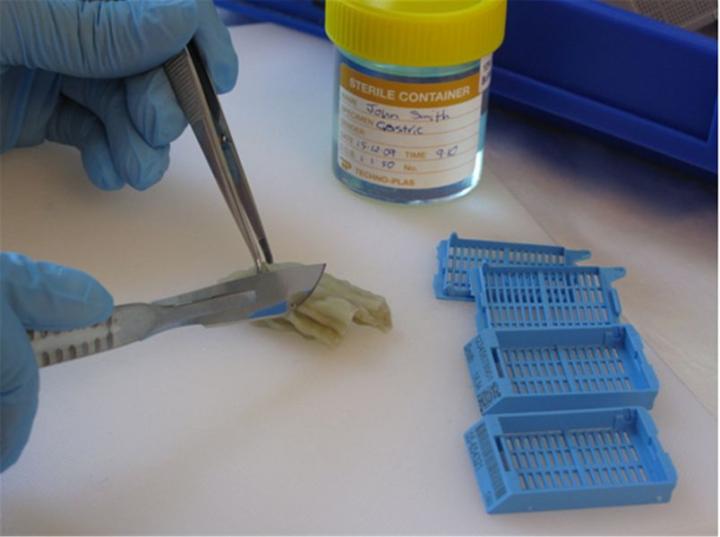
Zuschneiden
Der grobe Zuschnitt der Probe bedarf zunächst einer sorgfältigen Untersuchung und Beschreibung des vorhandenen Gewebes, in dem untersuchungsrelevante Abschnitte zu definieren sind. Größere Proben erfordern mitunter eine weitere Dissektion, bevor repräsentative Bereiche herausgeschnitten werden können. Die Anzahl der produzierten Gewebestücke, deren Abmessungen und Aussehen sind zu dokumentieren. Beispielsweise können mehrere Proben aus den Exzisionsrändern eines Tumors entnommen werden, um sicherzustellen, dass der Tumor vollständig entfernt wurde. Bei kleinen Proben kann der Zuschnitt entfallen und die gesamte Probe verarbeitet werden. Jene Gewebestücke, die zur Infiltration ausgewählt werden, sind in Kassetten zu deponieren, in kleine, perforierte Probenkörbe. Diese werden in Chargen zusammengefasst und als solche in den Infiltrationsautomaten geladen, wo sie mit Wachs infiltriert werden.
Gewebeinfiltration
Wenn große Probenchargen zu infiltrieren sind, kommen gemeinhin automatisierte Geräte zum Einsatz, die „Gewebeinfiltrationsautomaten“ heißen. Diese Geräte ermöglichen die sequentielle Infiltration der Proben mit verschiedenen Lösungsmitteln, bevor sie schließlich in geschmolzenes Paraffin überführt werden. Anfänglich entsprechen die Proben einer wässrigen Umgebung. Sie müssen entwässert und geklärt werden, was typischerweise in Ethanol und Xylol geschieht, um eine nicht wässrige Umgebung zu schaffen. Dabei ist zu berücksichtigen, dass geschmolzenes Wachs zwar flüssig, aber hydrophob und nicht mit Wasser mischbar ist – es könnte in die Proben nicht eindringen, beließe man sie in ihrem ursprünglichen Zustand. Die einzelnen Schritte und Dauer des Infiltrationsprotokolls hängen von der Art und Größe der Proben ab. Kleine Proben lassen sich in nur einer Stunde infiltrieren, während große Proben durchaus zwölf Stunden und mehr benötigen können. In vielen Labors wird vor allem über Nacht infiltriert. Außerdem besteht erheblicher Druck und eine entsprechende Tendenz, Infiltrationsautomaten zu verwenden, um kürzere Bearbeitungszeiten zu erreichen und den Arbeitsablauf zu verbessern.

Einbettung
Nach der Infiltration werden die Proben in eine Einbettstation überführt, wo sie aus ihren Kassetten entnommen und in mit Wachs gefüllte Schalen gelegt werden. Dabei ist die Position der Proben in der Einbettform zu beachten. Die Ausrichtung des Gewebes entscheidet darüber, in welcher Ebene geschnitten wird, und letztlich hängt davon ab, ob pathologisch verändertes Gewebe angemessen dargestellt wird und mikroskopisch beurteilt werden kann. Die Kassette, in der das Gewebe infiltriert wurde, ist so beschriftet, dass sie eine eindeutige Identifikation der Probe ermöglicht. Sie wird nun auf die Einbettform gelegt und durch Zugabe von weiterem Wachs an diese angeklebt. Der so entstehende „Block“ wird dann auf eine kalte Oberfläche überführt, wo er aushärten soll. Sobald das geschehen ist, kann die Einbettform abgenommen werden. Die Kassette, die jetzt mit Wachs gefüllt und Teil des Blocks ist, bietet eine stabile Basis für das Einspannen ins Mikrotom. Der Block, der die Probe enthält, kann nun geschnitten werden.

Schnitterstellung
Die Schnitte werden auf einem Präzisionsinstrument, dem Mikrotom, mit extrem dünnen Stahlklingen geschnitten. Paraffinschnitte werden gemeinhin bei einer Dicke von 3-5 µm erstellt, um sicherzustellen, dass im Schnitt nur eine einzige Zellschicht Platz findet. Um die Größenverhältnisse zu verdeutlichen: Ein rotes Blutkörperchen hat einen Durchmesser von etwa 7 µm. Einer der Vorteile von Paraffinwachs als Einbettmittel ist, dass die Schnitte beim Schneiden Kante an Kante aneinanderhaften und so ein Band von Schnitten bilden. Diese Schnittbänder machen die Handhabung der Präparate einfacher.
Nun lässt man die Schnitte in einem Wasserbad aufschwimmen, um sie zu glätten und dann von der Wasseroberfläche auf einen Objektträger aufzuziehen. Nach gründlicher Trocknung können die Präparate dann gefärbt werden.


Färbung
Abgesehen von einigen natürlichen Pigmenten wie Melanin, sind die Zellen und extrazellulären Komponenten der meisten Proben farblos. Um in der Hellfeldmikroskopie strukturelle Details bewerten zu können, ist es erforderlich, Gewebeelemente anzufärben. Die Routinefärbung, die als universeller Ausgangspunkt zum Erlangen wesentlicher struktureller Informationen dient, ist die Hämatoxylin-Eosin-Färbung, oft schlicht als H&E bezeichnet. Mit dieser Methode lassen sich Zellkerne blau färben und Zytoplasma und viele extrazelluläre Komponenten in rosa Farbtönen darstellen. In der Histopathologie können viele Erkrankungen allein durch die Untersuchung H&E-gefärbter Schnitte diagnostiziert werden. Manchmal jedoch sind zusätzliche Informationen erforderlich, die die Routinefärbung nicht hergibt. Dann bedarf es anderer Färbungen, um eine endgültige Diagnose zu stellen. Dabei kann es sich um Spezialfärbungen handeln, die unter Verwendung von Farbstoffen oder Metallen bestimmte Strukturen oder Mikroorganismen definieren, oder um immunhistochemische Methoden (IHC), die auf markierte Antikörper setzen, um diagnostisch relevante Proteine zu lokalisieren. Darüber hinaus können molekulare Methoden wie die In-situ-Hybridisierung (ISH) erforderlich werden, um spezifische DNA- oder RNA-Sequenzen nachzuweisen. All diese Methoden können auf Paraffinschnitte angewendet werden und in den meisten Fällen sind die probetragenden Objektträger vollständig stabil und lassen sich jahrelang aufbewahren.
Nach der Färbung werden die Schnitte mit einem Deckglas bedeckt und dann an einen Pathologen gegeben, der sie unter dem Mikroskop betrachtet, um zu einer Diagnose zu gelangen und einen Bericht zu erstellen.

About the presenter

Geoffrey Rolls is a Histology Consultant with decades of experience in the field. He is a former Senior Lecturer in histopathology in the Department of Laboratory Medicine, RMIT University in Melbourne, Australia.
Related Content
Die Inhalte des Knowledge Pathway von Leica Biosystems unterliegen den Nutzungsbedingungen der Website von Leica Biosystems, die hier eingesehen werden können: Rechtlicher Hinweis. Der Inhalt, einschließlich der Webinare, Schulungspräsentationen und ähnlicher Materialien, soll allgemeine Informationen zu bestimmten Themen liefern, die für medizinische Fachkräfte von Interesse sind. Er soll explizit nicht der medizinischen, behördlichen oder rechtlichen Beratung dienen und kann diese auch nicht ersetzen. Die Ansichten und Meinungen, die in Inhalten Dritter zum Ausdruck gebracht werden, spiegeln die persönlichen Auffassungen der Sprecher/Autoren wider und decken sich nicht notwendigerweise mit denen von Leica Biosystems, seinen Mitarbeitern oder Vertretern. Jegliche in den Inhalten enthaltene Links, die auf Quellen oder Inhalte Dritter verweisen, werden lediglich aus Gründen Ihrer Annehmlichkeit zur Verfügung gestellt.
Vor dem Gebrauch sollten die Produktinformationen, Beilagen und Bedienungsanleitungen der jeweiligen Medikamente und Geräte konsultiert werden.
Copyright © 2026 Leica Biosystems division of Leica Microsystems, Inc. and its Leica Biosystems affiliates. All rights reserved. LEICA and the Leica Logo are registered trademarks of Leica Microsystems IR GmbH.