Digitale Pathologie



Was ist digitale Pathologie?
Die digitale Pathologie umfasst die Erfassung, Verwaltung, Weitergabe und Interpretation von pathologischen Informationen, einschließlich Objektträgern und Daten, in einer digitalen Umgebung. Digitale Objektträger werden erstellt, wenn Glasobjektträger über einen Scanner erfasst werden, der ein hochauflösendes digitales Bild produziert, das auf einem Computerbildschirm oder Mobilgerät angezeigt werden kann.
Inhaltsverzeichnis
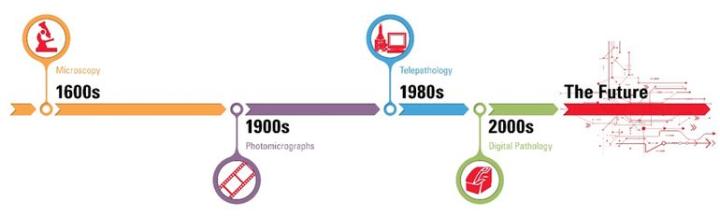
Die Nutzung automatisierter Scanner für die digitale Pathologie macht es möglich, bei hohem Durchsatz vollständige Glasobjektträger als Hellfeld- oder fluoreszenzmikroskopische Aufnahmen zu erfassen, wobei die Vergrößerung mit der am Standardmikroskop vergleichbar ist. Zum sicheren Teilen digitaler Objektträger im Netzwerk steht spezielle Software für die digitale Pathologie zur Verfügung. Darüber hinaus helfen Tools zur automatischen Bildanalyse bei der Interpretation und der Quantifizierung der Biomarkerexpression in Gewebeschnitten.
Die Geschichte der digitalen Pathologie reicht über 100 Jahre zurück, als zum ersten Mal spezielle Geräte verwendet wurden, um mikroskopische Bilder auf Fotoplatten zu übertragen. Das Konzept der Telepathologie, also dem Austausch mikroskopischer Aufnahmen zwischen entfernten Standorten, ist immerhin 50 Jahre alt. Und im vergangenen Jahrzehnt ließ sich eine regelrechte Transformation der Pathologie hin zur Digitalität beobachten: Immer mehr Prozesse werden von der analogen in eine digitale Umgebung hin verlagert.
Der rasche Fortschritt der Technologie zur Darstellung ganzer Objektträger (im Englischen als whole-slide imaging oder WSI bezeichnet) sowie die Weiterentwicklung in Bezug auf Softwareanwendungen, LIS/LIMS-Schnittstellen und Hochgeschwindigkeitsnetzwerke ermöglichen die vollständige Integration der digitalen Pathologie in alltägliche Arbeitsabläufe.
Die digitale Pathologie gestattet es Pathologen, sich unverzüglich und aus der Ferne Fällen zu widmen, Gewebe zu bewerten und dabei transparent und konsistent zu arbeiten, wodurch sich Effizienz und Produktivität steigern lassen. Die Zukunft der digitalen Pathologie mag von translationaler Forschung, computergestützten Diagnosen und personalisierter Medizin geprägt sein – und vielleicht von anderen Chancen, die wir heute noch nicht absehen.
Was sind die Vorteile der digitalen Pathologie?
Glasobjektträger sind nicht aus der Mode gekommen, und das aus gutem Grund. Die Pathologie nimmt ihren Anfang in der Gewebeprobe. Für diese Gewebeprobe werden Glasobjektträger gebraucht, auch wenn diese später digitalisiert werden. Moderne Pathologie allerdings ist viel mehr als Gewebe und Scans. Es geht darum, Qualität, Produktivität und weitere Parameter zu verbessern.
Schauen wir uns an, welchen Wandel die Pathologie von heute durchläuft:
- Es mangelt an Pathologen, wobei mehr Pathologen in den Ruhestand gehen als neue hinzukommen.
- Digitale Technologien werden immer besser an die Erfordernisse des Laboralltags angepasst und stehen heute schon für hohe Qualität und Innovation.
Die heutige Pathologie verlangt nach neuen Konzepten. Und wenn Pathologen sich scheuen, die digitale Pathologie voll und ganz anzunehmen, verpassen sie all die Möglichkeiten, die Glasobjektträger schlicht nicht bieten.
Die digitale Pathologie braucht Glasobjektträger und hat doch zahlreiche Vorteile ihnen gegenüber. Das wird bereits beim simplen Vergleich der Betrachtung eines Gewebeschnitts unter dem Mikroskop und im digitalen Netzwerk deutlich.
Die Qualität der Arbeit lässt sich mit digitaler Pathologie wie folgt erhöhen:
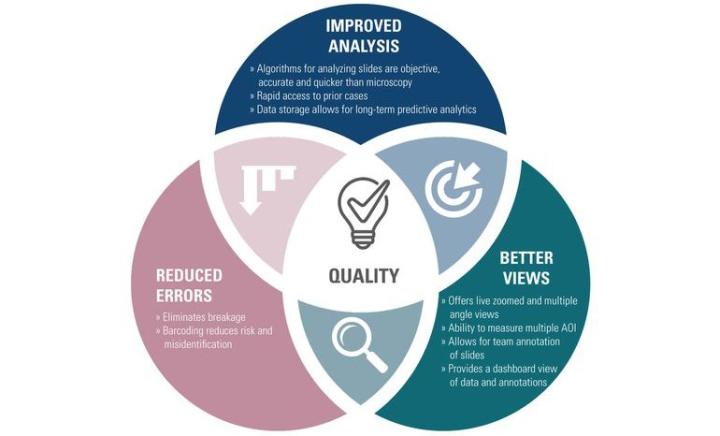
Verbesserte Analyse:
-
Algorithmen zur Analyse von Objektträgern sind objektiv, genau und schneller als die Mikroskopie
-
Schneller Zugriff auf frühere Fälle
- Datenspeicherung ermöglicht langfristige prädiktive Analysen
Weniger Fehler:
- Digitale Objektträger zerbrechen nicht
- Barcodes reduzieren das Risiko der Fehlidentifizierung
Stets klare Sicht:
- Live-Ansicht mit Zoom und mehreren Blickwinkeln
- Möglichkeit zur Messung mehrerer Gewebeausschnitte, die von diagnostischem Interesse sind
- Ermöglicht die Kommentierung von Objektträgern im Team
- Übersicht über sämtliche Daten und Anmerkungen im Dashboard
Einer der größten Vorteile der digitalen Pathologie sind die vielen Möglichkeiten, wie sie kurz- und langfristig zu einer Steigerung der Produktivität beiträgt:
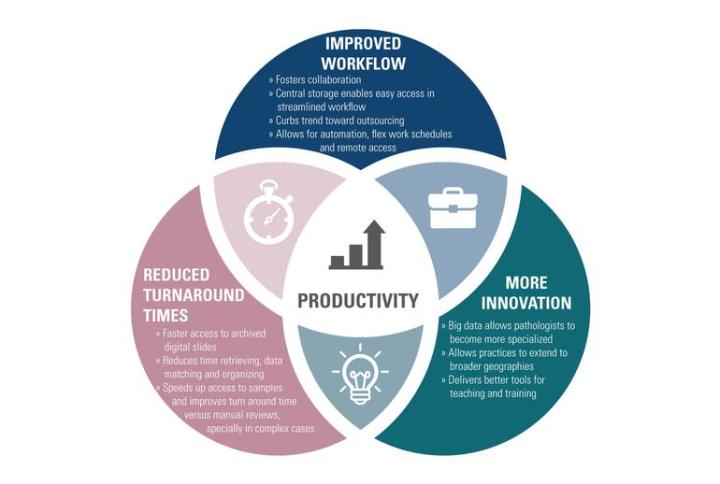
Optimierter Arbeitsfluss
- Fördert die Zusammenarbeit
- Zentrale Speicherung ermöglicht einfachen Zugriff und effiziente Arbeitsabläufe
- Begrenzt den Trend zum Outsourcing
- Ermöglicht Automatisierung, flexible Arbeitszeiten und Fernzugriff
Kürzere Bearbeitungszeiten:
- Schnellerer Zugriff auf archivierte digitale Objektträger
- Reduziert den Zeitaufwand zum Abrufen, zum Abgleich und der Organisation von Daten
- Beschleunigt den Zugriff auf Proben und reduziert die Zeit zur Diagnose- und Berichterstellung im Vergleich zum manuellen Verfahren, insbesondere bei komplexen Fällen
Mehr Innovation:
- Big Data vereinfachen die Spezialisierung der Pathologen
- Labore können einen geografisch größeren Bereich bedienen und so die Patientenversorgung verbessern
- Eignet sich hervorragend für Aus- und Weiterbildung
„Aber Glasobjektträger funktionieren doch gut“, hört man zuweilen im Sinne einer Rechtfertigung, nicht in die digitale Pathologie zu investieren. Dabei werden jedoch einige wichtige Punkte übersehen, unter anderem die langfristigen Kostenersparnisse, die die Digitalisierung mit sich bringt. Schauen wir uns ein paar Beispiele an.
- Kurierdienst nicht länger notwendig
- Effizienter, beschleunigter Arbeitsfluss
- Reiseaufwand für Gutachten und Zweitmeinung reduziert
- Möglichkeit zur geografischen Expansion bietet unzählige Chancen zur Erweiterung des Geschäftsmodells
- Reduziert die Notwendigkeit von Überstunden
In sieben Schritten zur digitalen Pathologie
Was der Umstellung zur digitalen Pathologie im Wege steht …
„Mit dem Mikroskop ist doch alles in Ordnung.“
„Unsere Informationssysteme sind mit den neuen Technologien nicht kompatibel.“
„Aller Anfang ist schwer.“
Das sind nur einige der Bedenken, die Pathologen hinsichtlich der digitalen Pathologie haben. Doch je tiefer sie in das Thema eintauchen, desto eher stellen sie fest, dass ihr Widerwille zur Digitalisierung sie von einem Fortschritt abhält, der mit vielen Vorteilen verbunden ist. Sie entdecken dann auch, dass die alten Methoden mit den digitalen Lösungen nicht konkurrieren können.
Und trotz aller Erkenntnis zu Chancen und Vorteilen, zu Genauigkeit, Bearbeitungszeiten, Effizienz und Zusammenarbeit, kostet der Schritt aus der analogen in die digitale Pathologie Überwindung.
Als Branchenführer in Lösungen für die digitale Pathologie kennen wir die Herausforderungen, die mit einer vollständigen Umstellung einhergehen.
Meist wird sie von einer Transformation der Organisation begleitet und damit diese zielführend bleibt, ist es wichtig, zu wissen, wie man am besten anfängt und welche Schritte zu gehen sind.
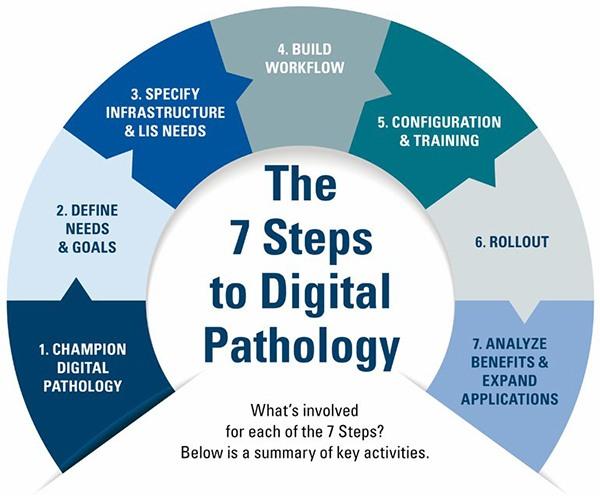
| SCHRITTE | AUFGABEN |
|---|---|
| 1. Die Herausforderung der digitalen Pathologie annehmen |
|
| 2. Bedürfnisse und Ziele definieren |
|
| 3. Anforderungen an Infrastruktur und Laborinformationssysteme (LIS) bestimmen |
|
| 4. Arbeitsfluss aufbauen |
|
| 5. Umstellung gestalten und Mitarbeiter schulen |
|
| 6. Umstellung |
|
| 7. Anwendungen analysieren und erweitern |
|
Welche zukünftigen Trends zeichnen sich für die digitale Pathologie und Immunhistochemie ab?

Die digitale Pathologie wird zunehmend von der pharmazeutischen Industrie und führenden klinischen Forschungsorganisationen verwendet, um Prozesse der Arzneimittelentwicklung zu rationalisieren, einschließlich der Wirkstofffindung, präklinischer und klinischer Studien.
Besondere Chancen bestehen für die mögliche zukünftige Nutzung der digitalen Pathologie zur quantitativen Analyse der aufkommenden therapiebegleitenden Diagnostik und neuartigen Theranostik. Dieses Feld gewinnt weiter an Bedeutung im Angesicht der Entwicklung von Assays, die mit dem menschlichen Auge kaum auszuwerten sind. Dazu zählen beispielsweise Multiplex-Assays, die diffuse Färbungen mehrerer zellulärer Kompartimente erzeugen, von denen vielleicht nur eine klinisch relevant ist.
Die zunehmende Komplexität solcher Assays treibt die Entwicklung digital-pathologischer Lösungen voran, die bei hohem Durchsatz und fortschrittlicher Erfassung von Hellfeld-, Fluoreszenz- und multispektralen Bildern eine Mustererkennung ermöglichen, um relevante Gewebetypen und Zellbestandteile zu identifizieren. Des Weiteren sollen sie zur Quantifizierung von immunhistochemischen Färbeintensitäten befähigen.
Ihren Ausdruck findet die beschriebene Entwicklung in der Bereitstellung digitaler Pathologiesysteme, die klinisch relevante diagnostische und prognostische Scores ausgeben, die auf einem Vergleich der aktuellen Analyseergebnisse mit einer aus klinischen Daten abgeleiteten Standardkurve beruhen. Hierin liegt bislang weitgehend ungenutztes Potenzial der digitalen Pathologie. Tatsächlich ließen sich die Informationen aus Standardaufnahmen, immunhistochemischen Verfahren und Modalitäten wie FACS und MALDI-TOF kombinieren, um eine diskretere Patientenstratifikation in klinisch relevante Gruppen zu erreichen. Es geht nicht darum, die Immunhistochemie zu ersetzen, sondern sie durch neue molekulare Tests und ergänzende diagnostische Werkzeuge zu erweitern, die sich zur Integration in die digitale Pathologie anbieten.
Die Revolutionierung von Aus- und Weiterbildung durch die digitale Pathologie
Der Bildungssektor gehörte zu den ersten Anwendern der digitalen Pathologie und setzte sie im gesamten Spektrum des histopathologischen Lernens ein, vom Studium über die kontinuierliche berufliche Weiterbildung bis hin zur externen Qualitätssicherung.
Die traditionelle Ausbildung an Lichtmikroskopen, unter denen Glasobjektträger betrachtet werden, konnte bestimmte Herausforderungen nie überwinden, etwa den Zugang zu Präparaten und die Standardisierung von Kursinhalten, was mit der digitalen Pathologie überhaupt kein Problem ist. Die Vorteile der digitalen Pathologie für die Aus- und Weiterbildung lassen sich wie folgt zusammenfassen:
- Standardisierung des Studienmaterials: Im digital-pathologischen Kurs sieht jeder Teilnehmer genau den gleichen Inhalt. Im Gegensatz dazu wurden bislang vor allem Glasobjektträger mit Schnitten eingesetzt, die zwar aus demselben Gewebeblock stammten, aber nicht notwendigerweise dieselben morphologischen Eigenschaften und Expressionsmuster aufwiesen. Die Standardisierung der Inhalte stellt sicher, dass jeder Teilnehmer die gleichen Lernmöglichkeiten hat. Sie erhöht die Qualität der Ausbildung und vereinfacht den Lernprozess für die Studierenden. Darüber hinaus erleichtert die digitale Pathologie die Behandlung seltener Fälle im Kurs, da nur eine digitale Kopie des Objektträgers erforderlich ist und nicht ein Glasobjektträger pro Teilnehmer.
- Vereinfachter Zugriff auf Präparate: Die digitale Pathologie ermöglicht einen besseren Zugriff auf objektträgerbasiertes Material, auch von außerhalb des Labors und nach Feierabend. Die Lernenden können über einen Standardbrowser, über PC, Tablet oder Smartphone auf ihre digitalen Kursinhalte zugreifen und damit jederzeit und von überall aus mit den Objektträgern arbeiten. Der Einsatz der digitalen Pathologie in der kontinuierlichen beruflichen Weiterbildung und externen Qualitätssicherung trägt zur effizienteren Arbeit und Kostenreduktion bei, da die Objektträger nicht mehr physisch von einem Ort zum anderen transportiert werden müssen, sondern gleichzeitig an mehreren Standorten betrachtet werden können.
- Möglichkeit zur Entwicklung neuer Lernstrategien: Der Wechsel von der physischen in die digitale Ausbildungsumgebung bietet viele Vorteile gegenüber den traditionellen histopathologischen Lehrmethoden auf Basis von Lichtmikroskopie und Glasobjektträgern. Es können mehrere digitale Objektträger gleichzeitig angezeigt und direkt verglichen werden, etwa zur Beurteilung immunhistochemischer Marker im gleichen Gewebeausschnitt (Abbildung 6).
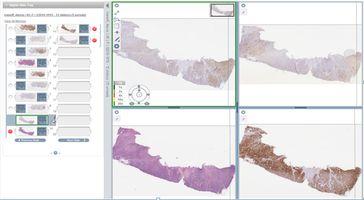
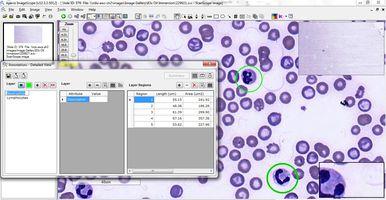
Für Pädagogen hingegen ist die eindeutige Identifikation relevanter Gewebeausschnitte auf Schnitt-, zellulärer und subzellulärer Ebene interessant, die sich mit Glasobjektträgern eher schwierig gestaltet – vor allem dann, wenn jeder Student etwas anderes sieht (Abbildung 7). Und mit spezieller Bildungssoftware für die digitale Pathologie können Fragen und Übungen in die digitalen Objektträger eingebettet werden, die kontextbezogene Informationen liefern und direkt auf jene Gewebe- und Zellmerkmale verweisen, auf die sie sich beziehen.
About the presenters

Sherri’ Heffner, CT(ASCP), has held clinical and research laboratory positions at private and academic institutions and sales/marketing positions with leading laboratory and technology companies, including Aperio.

Dr. Colgan has over a decade of experience in the digital pathology sector and is focused on how this new and disruptive technology can be leveraged to provide real benefits in both the healthcare and research domains. Prior to working with Leica Biosystems, she came from a research background with a BSc in Biotechnology and a PhD in Vascular Biology from Dublin City University, Ireland.

Colin Doolan has over ten years' experience working with Digital Pathology software solutions for Education, Research and Healthcare markets. He received his BSc in Biotechnology from Dublin City University, Ireland.
Related Content
Die Inhalte des Knowledge Pathway von Leica Biosystems unterliegen den Nutzungsbedingungen der Website von Leica Biosystems, die hier eingesehen werden können: Rechtlicher Hinweis. Der Inhalt, einschließlich der Webinare, Schulungspräsentationen und ähnlicher Materialien, soll allgemeine Informationen zu bestimmten Themen liefern, die für medizinische Fachkräfte von Interesse sind. Er soll explizit nicht der medizinischen, behördlichen oder rechtlichen Beratung dienen und kann diese auch nicht ersetzen. Die Ansichten und Meinungen, die in Inhalten Dritter zum Ausdruck gebracht werden, spiegeln die persönlichen Auffassungen der Sprecher/Autoren wider und decken sich nicht notwendigerweise mit denen von Leica Biosystems, seinen Mitarbeitern oder Vertretern. Jegliche in den Inhalten enthaltene Links, die auf Quellen oder Inhalte Dritter verweisen, werden lediglich aus Gründen Ihrer Annehmlichkeit zur Verfügung gestellt.
Vor dem Gebrauch sollten die Produktinformationen, Beilagen und Bedienungsanleitungen der jeweiligen Medikamente und Geräte konsultiert werden.
Copyright © 2026 Leica Biosystems division of Leica Microsystems, Inc. and its Leica Biosystems affiliates. All rights reserved. LEICA and the Leica Logo are registered trademarks of Leica Microsystems IR GmbH.