Fixierung und Fixiermittel (3) – Andere Fixiermittel als die üblichen Aldehyde

Neben Formaldehyd und Glutaraldehyd, die im vorherigen Teil der Serie besprochen wurden, wurde eine Reihe anderer Reagenzien zur Fixierung eingesetzt, manchmal in einfacher Lösung, aber oft auch als Wirkstoffkombinationen in Fixiergemischen. Die wichtigsten dieser alternativen Fixiermittel sollen in diesem dritten Teil beschrieben werden.
Acrolein
Acrolein oder Acrylaldehyd (H2C=CHCHO) reagiert mit Makromolekülen und bildet ähnlich wie Formaldehyd reversible Quervernetzungen. Tatsächlich konnte gezeigt werden, dass es mehr solcher Querverbindungen ausbildet als das Standardfixiermittel. Acrolein reagiert über seine Doppelbindung auch mit Fettsäuren. Obwohl Acrolein das Gewebe schnell durchdringt und sehr reaktiv ist, hat es keine breite Akzeptanz gefunden, weil seine Anwendung unangenehm ist. Acrolein stimuliert den Tränenfluss; zudem ist es bei alkalischem pH-Wert instabil und tendiert zur Polymerbildung. Seine wichtigsten Anwendungsgebiete sind die Enzymhistochemie und die Fixierung von pflanzlichem Material. Nach der Fixierung im Gewebe verbleibende Carbonylgruppen bewirken bei Anwendung von Techniken wie der PAS-Reaktion eine unerwünschte Hintergrundfärbung.1-3
Glyoxal
Glyoxal oder Diformyl (OHCCHO) ist ein bifunktionales Aldehyd, das ähnlich wie Formaldehyd reagiert und ein vergleichbares morphologisches Bild erzeugt. Beide Aldehydgruppen sind potenziell reaktiv und tragen zur Bildung von Quervernetzungen bei. Glyoxal ist der Hauptbestandteil in mehreren kommerziell erhältlichen Fixiermitteln, die besonders für die Mikrowellenfixierung, aber auch für Routinearbeiten empfohlen werden. Es wird gemeinhin als Formalinersatz bezeichnet, da es aufgrund seines extrem niedrigen Dampfdrucks bei Raumtemperatur praktisch nicht in den gasförmigen Zustand übergeht und deshalb als weniger gesundheitsgefährdend betrachtet wird. Obwohl es ein Reizstoff ist und bei Hautkontakt potenziell sensibilisierend wirkt, gilt Glyoxal derzeit nicht als Karzinogen. Nichtsdestotrotz sind auf den entsprechenden Produkten Warnhinweise ob seiner möglichen mutagenen Wirkungen angegeben. Es reagiert mit DNA und bildet dabei instabile Addukte. Glyoxal ist biologisch abbaubar, sodass seine Entsorgung weniger kompliziert ist als die von Formalin.2,4,5
Osmiumtetroxid
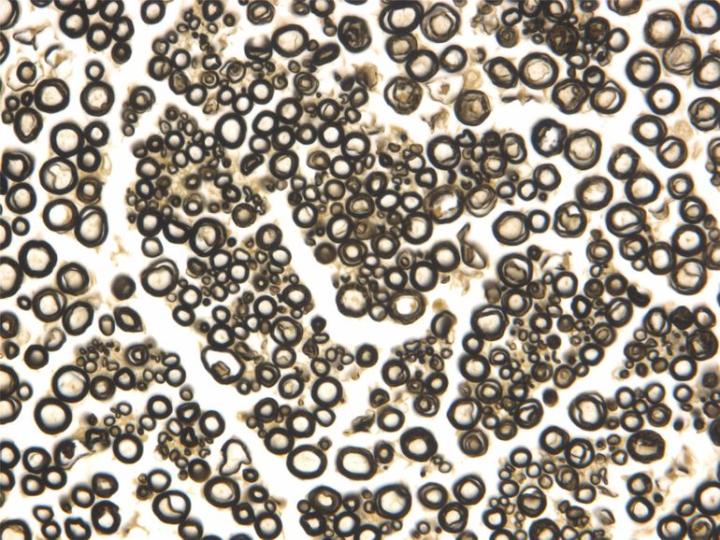
Osmiumtetroxid (OsO4) ist ein hochgiftiger, flüchtiger, kristalliner Feststoff, der in versiegelten Ampullen geliefert wird. Aufgrund seiner Volatilität darf die Substanz nur unter der Dunstabzugshaube gehandhabt werden, wobei alle Vorsichtsmaßnahmen zu treffen sind, um eine Exposition von Augen und Nase und damit eine Fixierung der Schleimhäute zu vermeiden.6 Osmiumtetroxid ist in polaren und unpolaren Lösungsmitteln löslich und reagiert mit den Seitenketten von Proteinen unter Bildung von Quervernetzungen. Die wichtigsten Fixierungsreaktionen von Osmiumtetroxid betreffen ungesättigte Bindungen in Lipiden und Phospholipiden, wobei hervorzuheben ist, dass es sich hier um eines der wenigen Fixiermittel handelt, das Lipide stabilisiert. Während der Fixierung wird Osmiumtetroxid zu unlöslichen, schwarzen Oxiden reduziert, die sich im Gewebe ablagern, insbesondere auf Membranen. Da Osmium ein Schwermetall ist, streut es Elektronen und erhöht die Elektronendichte im elektronenmikroskopischen Bild.7,8 Als En-Bloc-Färbung kann es zur lichtmikroskopischen Darstellung von Lipiden, vor allem von myelinisierten Nervenfasern, verwendet werden. Im Allgemeinen wird es bei etwa 1 % w/v als sekundäres Spezialfixiermittel für die Elektronenmikroskopie und für die Präparation von Nervenfasern genutzt.9
Carbodiimide:
Carbodiimide (RN=C=NR’) sind sehr reaktive Verbindungen, die mit verschiedenen funktionellen Gruppen reagieren. Diese Reaktionen lassen sich durch die Auswahl eines bestimmten Carbodiimids, durch pH-Wert, Temperatur und die Verwendung von Katalysatoren gezielt verstärken oder blockieren. Da sich während der Fixierung Peptidbindungen bilden und diese anschließend selektiv mit Proteasen aufgebrochen werden können, wird den Carbodiimiden ein gewisses Potenzial für die Verwendung in der Immunhistochemie und der routinemäßigen Histologie zugeschrieben. Zur Herstellung von Immunogenen werden sie bereits verwendet.2
Weitere vernetzende Fixiermittel
Diimidoester sind wasserlösliche Verbindungen, die die Aminogruppen von Proteinen quervernetzen und in Elektronenmikroskopie und Immunhistochemie Einsatz gefunden haben. Chloro-s-Triazine wie Cyanurchlorid hat man zur Darstellung der Muzine in Speicheldrüsen und zur Immunfluoreszenz verwendet. Diisocyanate hat man genutzt, um fluoreszierende Tags an Proteine anzubringen, während Diethylpyrocarbonat (DEPC) mit Tryptophanresten reagiert und in diesem Zusammenhang zur Dampffixierung von gefriergetrocknetem Gewebe dienen kann. In einer geeigneten Pufferlösung wurde es als Fixiermittel für kleine Proben vorgeschlagen. Maleimide scheinen Proteine querzuvernetzen und Benzoquinon reagiert mit Aminen, Aminosäuren und Peptiden, weshalb man es zur Peptidfixierung in der Immunhistochemie gebraucht hat.2,3
Quecksilberchlorid
Quecksilberchlorid (HgCl2) war eines der ersten Reagenzien, die zur Gewebefixierung genutzt wurden. In der älteren Literatur findet man häufig noch die Bezeichnung „ätzendes Sublimat“ und das ist ein durchaus passender Name, da es sich um eine korrosive Substanz handelt, die mit Metallen reagiert, einschließlich des Edelstahls, aus dem chirurgische Instrumente gefertigt sind. Obwohl die Mechanismen, die der Fixierung durch Quecksilberchlorid zugrunde liegen, nicht vollständig verstanden sind, ist zumindest bekannt, dass es mit Aminen, Amiden, Aminosäuren und Sulfhydrylgruppen reagiert. Letztere spielen vor allem bei Reaktionen mit Zystein eine Rolle, für die angenommen wird, dass sie zur Bildung von Quervernetzungen führen. Quecksilberchlorid wirkt stark koagulierend auf Proteine und versetzt das Gewebe in einen Zustand ausgeprägter Anfärbbarkeit mit sauren Farbstoffen. Es reagiert auch mit Phosphatresten in Nukleinsäuren und fixiert Nukleoproteine effektiv. Aus diesem Grund ist es der Hauptbestandteil von Fixiergemischen wie B5 und Helly’scher Lösung. Diese Fixiermittel werden vor allem dann empfohlen, wenn eine Notwendigkeit zur hochwertigen Kernkonservierung besteht, z. B. bei trepanierten Knochenmarkproben.
Die Verwendung von Fixiermitteln, die Quecksilberchlorid enthalten, ist jedoch mit wesentlichen Nachteilen verbunden. Die Substanz ist nicht nur korrosionsfördernd, sondern auch hochgiftig. Sie wird durch die Haut aufgenommen und kumuliert im Körper. In den meisten Ländern gelten strenge Vorschriften hinsichtlich der Entsorgung von Quecksilber und quecksilberhaltigen Verbindungen. Während der Fixierung mit Fixiergemischen, die Quecksilberchlorid enthalten, bildet sich zudem ein amorph-kristallines, grünlich-braunes Pigment, das sich als Artefakt auf der Probe ablagert. Erfolgt während der weiteren Verarbeitung und vor der Färbung eine Behandlung der Schnitte mit Jod, genauer gesagt mit Lugol‘scher Lösung, bildet sich Quecksilberjodid, das ausgewaschen werden kann. Überschüssiges Jod kann im Anschluss mit Natriumthiosulfat entfernt werden. Fixiermittel auf Quecksilberchloridbasis durchdringen das Gewebe nur schwer und wenn die Fixierung verlängert wird, um eine bessere Penetration zu erreichen, verhärten sich die Proben und werden anfällig, während der weiteren Verarbeitung zu schrumpfen.6,7
In den letzten Jahren wurde eine Reihe von Metallsalzen vorgestellt, die als Ersatz für Quecksilberchlorid dienen könnten, einschließlich Zink- und Bariumsalzen. Von diesen haben sich vor allem Zinkchlorid und Zinksulfat durchgesetzt, die in diesem Kontext als B5-Ersatzlösungen erhältlich sind.6
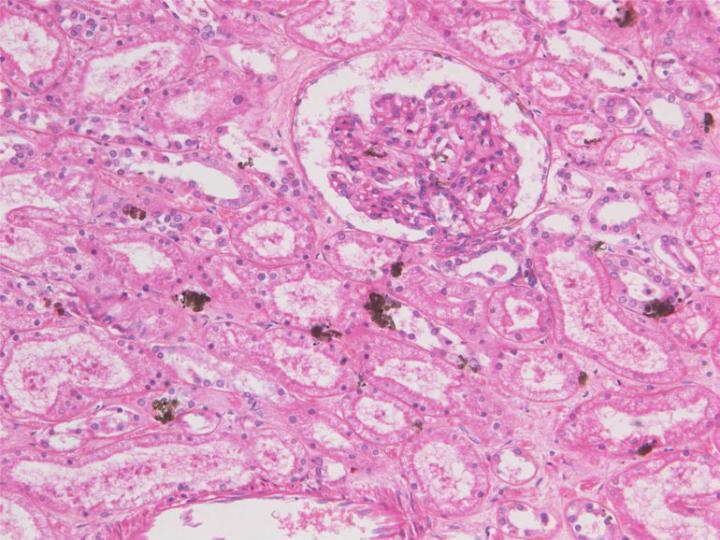
Zinksalze
Zinksulfat (ZnSO4) und Zinkchlorid (ZnCl2) ersetzen Quecksilberchlorid in zahlreichen kommerziell erhältlichen Fixiermitteln und Formulierungsempfehlungen. In der Regel wird Zinksulfat bevorzugt, weil es potenziell weniger korrosiv ist als Zinkchlorid, das mit Störungen von Gewebeinfiltrationsautomaten in Zusammenhang gebracht wurde6 (siehe Teil 4). Die Salze werden in Konzentrationen von etwa 1 % in 10%ige Formalinlösungen (wässrig oder alkoholisch, gepuffert oder ungepuffert) gegeben, wobei beim Ansetzen des Fixiermittels wiederholt über die Präzipitation von Zink oder Puffersalzen berichtet wurde. Zinksalze reagieren mit zahlreichen funktionellen Gruppen im Gewebe, darunter Amino-, Carboxyl- und Sulfhydrylgruppen. Die Bildung der jeweiligen Reaktionsprodukte ist reversibel; zum Teil lassen sie sich mit Zitrat oder EDTA auswaschen. Ähnlich wie Quecksilberchlorid soll auch Zink einen positiven Effekt auf die Fixierung und Färbung haben, insbesondere im Bereich der Zellkerne. Im Vergleich zu Formalin schreibt man den Zinksalzen Vorteile bei der Erhaltung der Immunreaktivität zu, wenn es mit Formalin allein verglichen wird, wodurch die Notwendigkeit zur Antigendemaskierung entfällt. Zinksalze sind weit weniger giftig als Quecksilbersalze und die Entsorgung von Zinklösungen ist problemlos möglich.2,6
Pikrinsäure
Pikrinsäure oder Trinitrophenol (C6H2(NO2)3OH) ist eine leuchtend gelbe, kristalline Substanz, die feucht gelagert werden muss, um einem möglichen Explosionsrisiko bei Erschütterungen oder dem Erhitzen der trockenen Substanz vorzubeugen. Sie sollte in einem dicht verschlossenen Behälter aufbewahrt und regelmäßig auf Feuchtigkeit hin überprüft werden.10 Wenn sie zu trocknen scheint, ist destilliertes Wasser hinzuzufügen. Zur Fixierung wird sie ausschließlich in Kombination mit anderen Wirkstoffen verwendet (siehe Teil 4 – Bouin‘sche und Hollande-Lösungen). Abgesehen von ihrer Verwendung in Fixiergemischen findet sich Pikrinsäure als saurer Farbstoff in mehreren Färbemitteln, z. B. in der van-Gieson-Lösung zur Muskelfärbung. Es verleiht Geweben während der Fixierung eine gelbe Farbe und sollte aufgrund seiner Azidität mit Ethanol 70 % ausgewaschen werden, bevor die Probe weiterverarbeitet wird. Wenn Pikrinsäurereste im Gewebe verbleiben, wirkt sich das nachteilig auf die Färbeeigenschaften des Gewebes aus, die mit der Zeit immer schlechter werden.
Pikrinsäure ist ein koagulierendes Fixiermittel, das die Ladungen an den ionisierbaren Seitenketten von Proteinen verändert und Ionenbindungen sowie Wasserstoffbrücken aufbricht. Die Koagulation beruht auf der Bildung von Salzen, sogenannten Pikraten, in Reaktionen mit den basischen Gruppen der Proteine. Pikrinsäure scheint weder Lipide noch Kohlenhydrate in wesentlichem Umfang zu fixieren, wird aber als Bestandteil von Fixiermitteln empfohlen, die der Konservierung von Glykogen dienen. Pikrinsäure kann Nukleinsäuren hydrolysieren, sodass von ihrer Verwendung abzusehen ist, wenn DNA oder RNA nachgewiesen werden sollen. Diese Substanz ist weiterhin in der Lage, kleinere Kalziumablagerungen im Gewebe zu lösen. Während der weiteren Verarbeitung von Proben, die in pikrinsäurehaltigen Reagenzien fixiert wurden, kommt es zu einer signifikanten Gewebeschrumpfung.6,7,11
Kaliumdichromat
Kaliumdichromat (K2Cr2O7) verhält sich wie ein nicht koagulierendes Fixiermittel, es sei denn, es wird bei einem pH-Wert von < 3,4-3,8 verwendet. Unter diesen Bedingungen reagiert es wie Chromsäure als koagulierendes Fixativ. Es ist Bestandteil mehrerer Fixiergemische (siehe Teil 4 – Zenker- und Helly‘sche Lösungen). Es wird angenommen, dass die Fixierung Redoxreaktionen zwischen Proteinen und Chromionen umfasst, wobei es zu einer gewissen Quervernetzung kommt, deren Umfang vom pH-Wert des Fixiermittels abhängt. Weiterhin sollen Chromionen mit den Carboxyl- und Hydroxylgruppen in den Seitenketten der proteinbildenden Aminosäuren reagieren. Die Aminogruppen bleiben frei, was die Färbung mit sauren Farbstoffen begünstigt. Weil Chromat mit ungesättigten Fetten reagiert und deren Löslichkeit mindert, gilt es als geeignetes Fixiermittel für Mitochondrien. Es wird generell empfohlen, chromatfixiertes Gewebe vor der weiteren Verarbeitung gründlich in Wasser zu waschen, um der Bildung eines unlöslichen Suboxids aus Ethanol und Chromat vorzubeugen. Traditionell hat man dichromathaltige Fixiermittel in histochemischen Verfahren zur Darstellung aminhaltiger, chromaffiner Elemente in endokrinen Geweben genutzt.6,7,11
Ethanol und Methanol
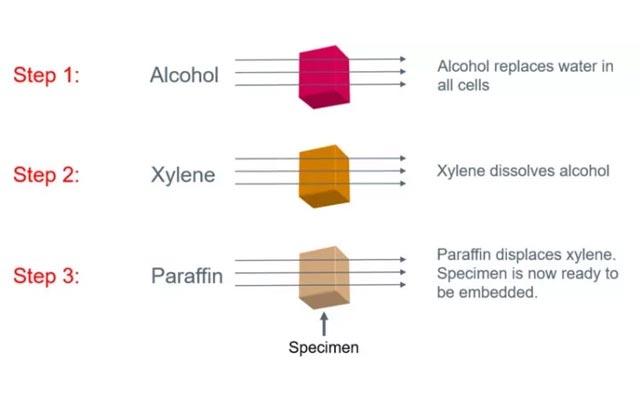
Ethanol (CH3CH2OH) und Methanol (CH3OH) gelten als proteindenaturierende Koagulanzien. Sie verdrängen das Wasser im Gewebe und interferieren so mit Wasserstoffbrücken und hydrophoben Bindungen. Innen liegende, hydrophobe Gruppen der Aminosäuren werden frei, woraus sich Veränderungen in der Tertiärstruktur des Proteins und seiner Löslichkeit ergeben. In seiner Struktur ist Methanol dem Wasser ähnlicher als Ethanol, weshalb die oben beschriebene Interferenz mit den Bindungen unter Ethanol stärker ist. Fixierungseffekte stellen sich ab einer Konzentration von 50-60 % für Ethanol und > 80 % für Methanol ein. Ethanol wird manchmal zur Glykogenkonservierung genutzt, führt aber zu einer Verzerrung der nukleären und zytoplasmatischen Details. Während Methanol ein gängiges Fixiermittel für Blutausstriche ist, setzt man 95%igen Ethanol zur Fixierung zytologischer Abstriche ein. Zur Fixierung von Gewebeproben allerdings werden beide Alkohole in der Regel mit anderen Reagenzien kombiniert.3,7,12
Aceton
Aceton (CH3COCH3) hat eine ähnliche Wirkung wie Alkohol und kann in der Präparation mikroskopischer Proben als Fixier- und Entwässerungsmittel genutzt werden. Besonders bei der schnellen Verarbeitung kleinerer Proben von Hand greift man auf Aceton zurück. Es wird weithin für die Fixierung von Proben empfohlen, die für die Darstellung von Enzymen vorgesehen sind. Dazu wird es in der Regel auf 4 °C gekühlt. Als effektives, schnell wirkendes Lösungsmittel für Lipide kann es das Gewebe sehr spröde machen. Da es zudem hochflüchtig und entzündlich ist, sieht man von seinem Einsatz in Gewebeinfiltrationsautomaten meist ab.3, 7
In diesem Zusammenhang sollen die nachteiligen Effekte des Acetons auf die Dichtungen und andere Komponenten der Geräte nicht unerwähnt bleiben.
Essigsäure
Essigsäure (CH3COOH) wirkt koagulierend auf Nukleinsäuren, fixiert aber keine Proteine. Ihre konservierende Wirkung auf Nukleinsäuren ist einer der Gründe für den Einsatz von Essigsäure in Fixiergemischen. Außerdem bewirkt Essigsäure eine Schwellung von Kollagen, womit der durch andere Inhaltsstoffe induzierten Schrumpfung entgegengewirkt werden kann. Essigsäure dringt sehr schnell in das Gewebe ein, hat aber einen hämolytischen Effekt.3,7
About the presenter

Geoffrey Rolls is a Histology Consultant with decades of experience in the field. He is a former Senior Lecturer in histopathology in the Department of Laboratory Medicine, RMIT University in Melbourne, Australia.
Referenzen
- Culling CFA, Allison RT and Barr WT eds. Cellular Pathology Technique. London: Butterworths, 1985.
- Eltoum I, Fredenburgh J, Grizzle WE. Advanced concepts in fixation: 1. Effects of fixation on immunohistochemistry, reversibility of fixation and recovery of proteins, nucleic acids, and other molecules from fixed and processed tissues. 2. Developmental methods of fixation. J Histotechnol 2001;24;201-210.
- Leong AS-Y. Fixation and fixatives. In Woods AE und Ellis RC eds. Laboratory histopathology. New York: Churchill Livingstone, 1994;4.1-1 - 4.1-26.
- Fisher Scientific. MSDS Glyoxal, 2008; http://fscimage.fishersci.com/msds/01960.htm; November 22, 2011.
- World Health Organization. Concise International Chemical Assessment Document 57 GLYOXAL. 2004; http://whqlibdoc.who.int/publications/2004/924153057X.pdf; November 22, 2011.
- Carson FL. Histotechnology. 2nd ed. Chicago: ASCP Press, 2007.
- Eltoum I, Fredenburgh J, Myers RB, Grizzle WE. Introduction to the theory and practice of fixation of tissues. J Histotechnol 2001;24;173-190.
- Bozzola JJ, Russell LD. Electron microscopy: principles and techniques for biologists. Boston: Jones und Bartlett, 1992.
- Lowe J. Techniques in neuropathology. In Bancroft JD and Stevens A eds. Theory and practice of histological techniques. New York: Churchill Livingstone, 1996.
- Sigma-Aldrich. MSDS Picric acid solution, 2011;November 22, 2011
- Drury RAB, Wallington EA. Carleton's histological technique. 5th ed. New York: Churchill Livingstone, 1980.
- Lillie RD, Fullmer HM. Histopathologic technique and practical histochemistry. 4th ed. New York: McGraw-Hill, 1976.
Related Content
Die Inhalte des Knowledge Pathway von Leica Biosystems unterliegen den Nutzungsbedingungen der Website von Leica Biosystems, die hier eingesehen werden können: Rechtlicher Hinweis. Der Inhalt, einschließlich der Webinare, Schulungspräsentationen und ähnlicher Materialien, soll allgemeine Informationen zu bestimmten Themen liefern, die für medizinische Fachkräfte von Interesse sind. Er soll explizit nicht der medizinischen, behördlichen oder rechtlichen Beratung dienen und kann diese auch nicht ersetzen. Die Ansichten und Meinungen, die in Inhalten Dritter zum Ausdruck gebracht werden, spiegeln die persönlichen Auffassungen der Sprecher/Autoren wider und decken sich nicht notwendigerweise mit denen von Leica Biosystems, seinen Mitarbeitern oder Vertretern. Jegliche in den Inhalten enthaltene Links, die auf Quellen oder Inhalte Dritter verweisen, werden lediglich aus Gründen Ihrer Annehmlichkeit zur Verfügung gestellt.
Vor dem Gebrauch sollten die Produktinformationen, Beilagen und Bedienungsanleitungen der jeweiligen Medikamente und Geräte konsultiert werden.
Copyright © 2024 Leica Biosystems division of Leica Microsystems, Inc. and its Leica Biosystems affiliates. All rights reserved. LEICA and the Leica Logo are registered trademarks of Leica Microsystems IR GmbH.