
Fixierung und Fixiermittel (2) – Faktoren, die die chemische Fixierung beeinflussen, Formaldehyd und Glutaraldehyd

Dieser zweite Teil der Serie „Fixierung und Fixiermittel“ beschäftigt sich mit den Faktoren, die die Geschwindigkeit und Effektivität der Gewebefixierung beeinflussen, und liefert detaillierte Informationen zu zwei häufig verwendeten Fixiermitteln: zu Formaldehyd, das in der Histologie Einsatz findet, und zu Glutaraldehyd, das für ultrastrukturelle elektronenmikroskopische Studien genutzt wird.
Faktoren, die die chemische Fixierung beeinflussen
Es gibt eine Reihe von Faktoren, die die Geschwindigkeit und Effektivität der Gewebefixierung beeinflussen.
Temperatur: Bei erhöhter Temperatur des Fixiermittels nehmen die Diffusionsrate und die Geschwindigkeit der chemischen Reaktionen zwischen dem Fixiermittel und den Gewebeelementen zu. Potenziell erhöht sich bei höheren Temperaturen aber auch die Geschwindigkeit von Degenerationsprozessen in nicht fixierten Bereichen der Probe. In Vorbereitung auf lichtmikroskopische Untersuchungen wird normalerweise bei Raumtemperatur fixiert. Optional kann eine weitere Fixierung bei Temperaturen bis zu 45°C erfolgen, wozu in der Regel der Infiltrationsautomat genutzt wird. Das ist so etwas wie eine Kompromisslösung, die weithin akzeptiert zu sein scheint und morphologische Details gut erhält. Bei der Fixierung in der Mikrowelle werden höhere Temperaturen erreicht, bis zu 65°C, jedoch nur für relativ kurze Zeiträume. Siehe Teil 5 für weitere Informationen.
Zeit: Die optimale Fixierungszeit hängt vom Fixiermittel ab. Für eine vollständige Fixierung muss das Fixiermittel durch Diffusion bis ins Zentrum der Probe vordringen und darüber hinaus muss genügend Zeit für die chemischen Reaktionen der Fixierung eingeräumt werden. Diffusions- und Reaktionszeit hängen vom verwendeten Reagens ab, weshalb die ideale Fixierungszeit von Fixiermittel zu Fixiermittel variiert. In klinischen Laboren, aber auch sonst bei hoher Auslastung, besteht ein erheblicher Druck, die Durchlaufzeiten zu reduzieren, um schneller Ergebnisse zu liefern. Dabei wird nicht selten unzureichend fixiertes Gewebe infiltriert. Das kann zu minderwertigen Schnitten führen, in denen das Gewebe verzerrt und schlecht angefärbt ist. Wenn eine unvollständig fixierte Probe in Ethanol überführt wird, setzt der Alkohol die Fixierung fort. Das ethanolfixierte Gewebe im Zentrum unterscheidet sich dann morphologisch von den äußeren Bereichen.
Penetrationsrate: Die Penetrationsrate eines Fixiermittels hängt von seinen Diffusionseigenschaften ab und variiert zwischen den verschiedenen Reagenzien. Wie von Medawar beschrieben, lässt sie sich nach der Formel d = K√t berechnen, wobei d die Penetrationstiefe, K der Diffusionskoeffizient und t die Zeit ist. Der Diffusionskoeffizient ist spezifisch für das verwendete Fixiermittel.1 Für die Praxis kann man annehmen, dass der Diffusionskoeffizient K der Distanz in Millimetern entspricht, über die das Fixiermittel in einer Stunde in das Gewebe eindringt. Für Formalin (10 %) ist K = 0,78. Das bedeutet, dass dieses Fixiermittel nicht mehr als 1 mm/Stunde in das Gewebe vordringt und es ungefähr 25 Stunden dauert, bis es im Zentrum einer Probe ankommt, die 10 mm dick ist (Distanz = 5 mm in 5² Stunden).

Abmessungen der Probe: Die oben angestellten Berechnungen unterstreichen die Bedeutung der Abmessungen der Probe für deren Fixierung. Eine Probe sollte nicht mehr als 4 mm dick sein.Im Idealfall wird aus der Probe eine 3 mm dicke Scheibe geschnitten, die sich optimal fixieren und infiltrieren lässt. Übrigens haben die Standardkassetten zur Gewebeinfiltration eine Tiefe von 5 mm.
Volumenverhältnis Fixiermittel zu Probe: Es ist wichtig, das Fixiermittelvolumen um ein Vielfaches größer zu wählen als das Probenvolumen. Das hängt damit zusammen, dass sich das Fixiermittel während der Fixierung verbraucht, in seiner Konzentration also abnimmt. Wird nur wenig Fixiermittel angeboten, wirkt sich das signifikant und nachteilig auf die Fixierung aus. Ein Verhältnis von 20 : 1 wird als das niedrigste akzeptable Verhältnis betrachtet; ein Verhältnis von 50 : 1 ist anzustreben.
pH und Puffer: Auf lichtmikroskopischer Ebene scheint der pH-Wert des Fixiermittels die Qualität der Gewebekonservierung kaum zu beeinflussen, was daran ersichtlich wird, dass einige Formulierungen einen ziemlich niedrigen pH-Wert haben, z. B. jene, die Essigsäure oder Pikrinsäure enthalten. Ein schlecht eingestellter pH-Wert kann jedoch andere Folgen haben, wie es für Formaldehydlösungen gilt. Hier bedeutet der Abbau von Formaldehyd zu Ameisensäure eine wesentliche Ansäuerung und diese saure Lösung reagiert mit Hämoglobin, wobei Formalinpigment als Artefakt entsteht. Heute werden Formaldehydlösungen deshalb auf einen pH-Wert von 6,8-7,2 gepuffert. Für die Elektronenmikroskopie hat der pH-Wert eine größere Bedeutung und sollte auf den physiologischen Wert eingestellt werden.2
Osmolalität: Auch die osmotischen Wirkungen des Fixiermittels sind auf der ultrastrukturellen Ebene bedeutsamer als für lichtmikroskopische Studien, weil es vor allem die Phospholipidmembranen sind, die leicht durch hypotone oder hypertone Lösungen beschädigt werden. Nichtsdestotrotz sollte die Osmolalität der Fixierlösung auch in der Routinehistologie nicht vernachlässigt werden. Im Allgemeinen ist es die Osmolalität des Vehikels, also des Puffers, die entscheidend ist. In einigen Formulierungen wird sie deshalb den physiologischen Gegebenheiten angepasst, z. B. bei Formalin in isotoner Kochsalzlösung. Bevor die Fixierung stattfindet, sind die Zellen sehr empfindlich gegenüber Abweichungen in der Isotonie. Wenn Proben nicht sofort fixiert werden können und feucht gehalten werden müssen, nutzt man deshalb isotone Kochsalzlösung. Allerdings ist es keine gute Idee, die Proben für längere Zeit in Kochsalzlösung aufzubewahren.
Fixiermittel
Es gibt eine Reihe von Reagenzien, die zur Gewebefixierung verwendet werden können. Formaldehyd, bei weitem das beliebteste Fixiermittel in der Histopathologie, und Glutaraldehyd, besonders geeignet für ultrastrukturelle Untersuchungen am Elektronenmikroskop, sollen hier beschrieben werden. Weitere Fixiermittel werden in Teil 3 besprochen.
Formaldehyd: Formaldehyd (CH2O) ist das einzige gasförmige Aldehyd und wird in Wasser gelöst, bis bei 37–40 % w/v eine Sättigung erreicht ist. Die so entstehende Lösung wird im Allgemeinen als „Formalin“ oder „konzentrierte Formaldehydlösung“ bezeichnet. Zur Fixierung wird ein Teil Formalin mit neun Teilen Wasser oder Puffer verdünnt. So erhält man eine 10%ige Formalinlösung, die etwa 4 % Formaldehyd w/v enthält – eine optimale Konzentration für die Fixierung. In konzentrierten Lösungen liegt Formaldehyd als Formaldehyd-Monohydrat (Methylenglykol) und in Form niedermolekularer Oligomere vor. In der verdünnten Lösung dominiert das Monohydrat. Paraformaldehyd, ein Polymer des Formaldehyds, kann in konzentrierten Formaldehydlösungen als weißer Niederschlag auftreten. Um die Polymerisation zu verhindern, wird der Lösung bis zu 15 % Methanol hinzugefügt. Andererseits kann Paraformaldehyd als trockenes Pulver gekauft und zur Herstellung von hochreinen Formaldehydlösungen verwendet werden, wie sie für die Elektronenmikroskopie benötigt werden.2, 3
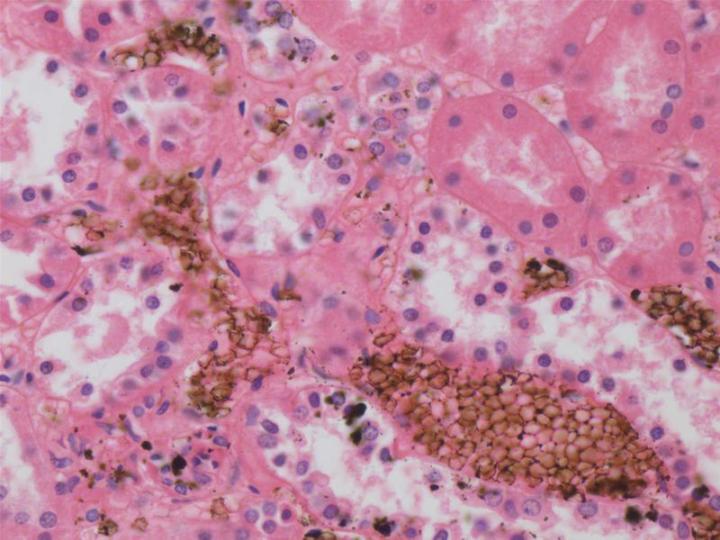
Ungepuffertes Formalin oxidiert langsam zu Ameisensäure, wodurch der pH-Wert sinkt. Derart saures Formalin kann unter Bildung eines braun-schwarzen Pigments mit dem Hämoglobin der Probe reagieren. Man spricht von Formalinpigment; aufgrund des höheren Hämoglobingehalts ist es in blutreichen Geweben besonders gut erkennbar. Dieses Pigment behindert die Diagnostik, da es mit pathologischen Pigmenten oder Mikroorganismen verwechselt werden kann.4 Obwohl das Pigment vor der Färbung vom Schnitt entfernt werden kann, ist dazu eine Behandlung mit gesättigter wässriger Pikrinsäure erforderlich und es ist vorzuziehen, seine Bildung von vornherein zu vermeiden. Deshalb, und weil Formaldehyd bei einem neutralen pH-Wert am effektivsten wirkt, werden Formalinlösungen normalerweise auf einen pH-Wert von 6,8-7,2 gepuffert.
Formaldehyd reagiert mit den Seitenketten von Proteinen, wobei reaktive Hydroxymethylgruppen gebildet werden. Es kann Kernproteine und Nukleinsäuren durchdringen und deren Nukleotide modifizieren, indem es mit freien Aminogruppen reagiert. Eine eventuell vorhandene Proteinhülle, wie sie bei Viren besteht, wird durch Formaldehyd stabilisiert. Weiterhin kann Formaldehyd mit den funktionellen Gruppen ungesättigter Fette reagieren, insbesondere wenn Kalziumionen vorhanden sind, während es sich Kohlenhydraten gegenüber eher inert verhält.5 Die Aminosäuren Lysin, Arginin, Zystein, Tyrosin, Threonin, Serin und Glutamin tragen Gruppen, die mit Formaldehyd reaktive Komplexe bilden. Diese wiederum können sich über Methylenbrücken quervernetzen und je länger eine Probe in Formalin liegt, desto mehr Brücken bilden sich.5 Während einige der beschriebenen Reaktionen reversibel sind und beim Waschen der Probe nach der Fixierung aufgehoben werden, bleiben die Querverbindungen im Wesentlichen bestehen.6 Seine Fähigkeit zur Konservierung der Peptide zellulärer Proteine hat Formaldehyd zu diesem universell einsetzbaren Fixiermittel gemacht, als das wir es heute kennen.
Die Verwendung von Formaldehyd ist nicht ohne gesundheitliche Gefahren, insbesondere bei Kontakt zu Augen und Haut oder Exposition über die Atemwege. Es ist reizend, ätzend und wirkt als Kontaktallergen. 1981 wurde Formaldehyd als wahrscheinlich karzinogen eingestuft, seit 2011 gilt es erwiesenermaßen als krebserregend.7, 8 Studien haben gezeigt, dass Formaldehyd bösartige Tumore des Nasopharynx und der Nasennebenhöhlen sowie myeloische Leukämien verursacht. Aus diesen Gründen gelten in den meisten Ländern strenge Richtlinien, um die Exposition gegenüber Formaldehyd am Arbeitsplatz zu begrenzen. In den USA beispielsweise beträgt der zulässige Expositionsgrenzwert 0,75 ppm (Durchschnitt über acht Stunden) und die zulässige Maximalexposition 2 ppm (über maximal 15 Minuten), und diese Empfehlungen werden durch ein Programm zur Überwachung der Formaldehydexposition unterstützt. In einem gut ausgestatteten Labor mit modernem Dunstabzug sollten diese Maximalwerte nicht überschritten werden.9, 10
Trotz der Risiken, die die Verwendung von Formaldehyd mit sich bringt, kann mit Sicherheit behauptet werden, dass sich die meisten Histologen und Pathologen ihr Wissen über gesundes und krankes Gewebe durch das Studium formalinfixierter Proben angeeignet haben. Aufgrund des zunehmenden Bewusstseins für die Toxizität dieses Reagens haben viele Labore nach einer sichereren Alternative gesucht und tun dies auch weiterhin. Alternativen zu Formalin werden in erster Regel nach ihrer Fähigkeit beurteilt, ein morphologisches Bild zu produzieren, das dem von formalinfixiertem Gewebe ähnlich oder sogar noch besser ist, und dabei nicht mit anschließenden Färbungen zu interferieren. Zu berücksichtigen sind dabei alle gängigen Färbungen einschließlich molekularer Methoden. Und der Preis der Alternative. Mit einem Wort, die meisten Labore verwenden weiterhin Formalin, da bislang kein zufriedenstellender Ersatz gefunden werden konnte. Daher ist es umso wichtiger, dass sich die Mitarbeiter der damit verbundenen Gefahren bewusst sind. Einige Alternativen zu Formaldehyd werden in Teil 3 besprochen.
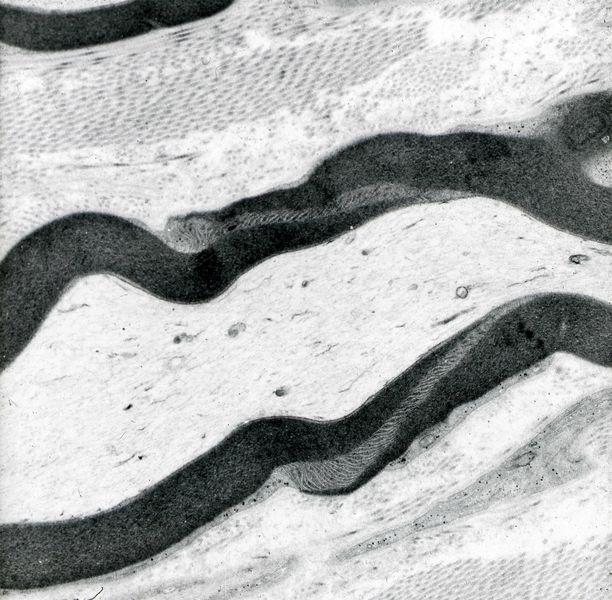
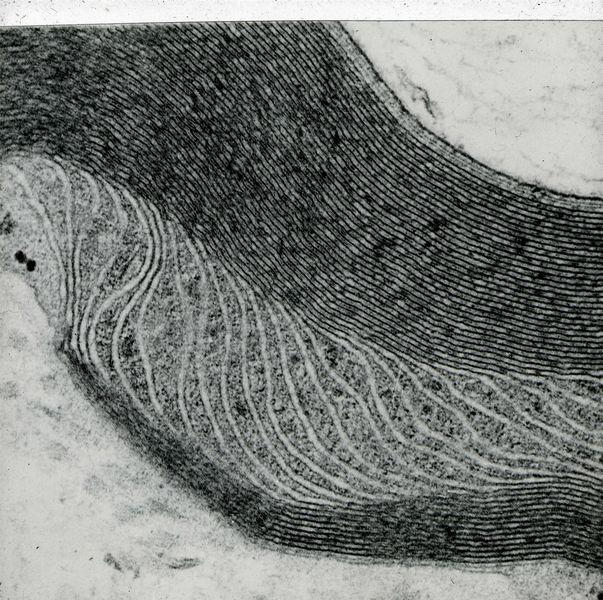
Glutaraldehyd: Glutaraldehyd oder glutarisches Dialdehyd (CHO(CH2)3CHO) besitzt Aldehydgruppen an beiden Enden des Moleküls und wird deshalb als bifunktionales Aldehyd angesehen. Beide Gruppen gehen Reaktionen mit denselben funktionellen Gruppen ein wie Formaldehyd, wobei Additionsverbindungen und Methylenbrücken gebildet werden. Aber auch ein einziges Glutaraldehydmolekül ist in der Lage, eine Querverbindung herzustellen, wenn es die sterische Anordnung der Reaktionspartner zulässt. Die Aminogruppen von Lysin sind in dieser Hinsicht besonders wichtig. In Glutaraldehyd fixiertes Gewebe ist umfassender quervernetzt als Proben, die in Formalin fixiert wurden. Allerdings reagieren nicht alle Aldehydgruppen und freibleibende Gruppen können, sofern sie nicht blockiert werden, bei Methoden wie der PAS-Reaktion eine unerwünschte Hintergrundfärbung verursachen. Die umfangreiche Vernetzung wirkt sich weiterhin negativ auf immunhistochemische Färbungen aus, bietet jedoch eine hervorragende Konservierung der zellulären Ultrastruktur. Das erklärt, warum Glutaraldehyd als Fixiermittel für die Elektronenmikroskopie so beliebt ist und warum in der Lichtmikroskopie Formaldehyd bevorzugt wird. Die durch Glutaraldehyd induzierten Quervernetzungen sind weitgehend irreversibel. Glutaraldehyd dringt nur sehr langsam ins Gewebe ein, weshalb für Probenscheiben eine maximale Dicke von 1 mm empfohlen wird.5, 11
Glutaraldehyd zersetzt sich langsam zu Glutarsäure und polymerisiert auch zu zyklischen und oligomeren Verbindungen. Glutaraldehyd sollte darum stabilisiert und in versiegelten Ampullen erworben werden. Zum Einsatz in der Elektronenmikroskopie wird es dann mit einem geeigneten Puffer angesetzt, sodass eine 3%ige Glutaraldehydlösung entsteht. Meist werden Cacodylat-, Phosphat- oder Maleatpuffer bei einem pH-Wert von 7,2-7,4 verwendet. In Vorbereitung auf elektronenmikroskopische Untersuchungen folgt auf die Primärfixierung mit Glutaraldehyd üblicherweise eine Sekundärfixierung in Osmiumtetroxid. In der Routinehistologie spielt Glutaraldehyd keine Rolle.11
About the presenter

Geoffrey Rolls is a Histology Consultant with decades of experience in the field. He is a former Senior Lecturer in histopathology in the Department of Laboratory Medicine, RMIT University in Melbourne, Australia.
Referenzen
- Medawar PB. The rate of penetration of fixatives. J Royal Micros Soc 1941;61;46-57.
- Carson FL. Histotechnology. 2nd ed. Chicago: ASCP Press, 1997.
- Leong AS-Y. Fixation and fixatives. In Woods AE and Ellis RC eds. Laboratory histopathology. New York: Churchill Livingstone, 1994;4.1-1 - 4.1-26.
- Rolls GO, Farmer NJ, Hall JB. Artefacts in histological and cytological preparations. In Woods A and Ellis R eds. Laboratory histopathology. New York: Churchill Livingstone, 1994;5.3-1 - 5.3-29.
- Eltoum I, Fredenburgh J, Myers RB, Grizzle WE. Introduction to the theory and practice of fixation of tissues. J Histotechnol 2001;24;173 -190.
- Eltoum I, Fredenburgh J, Grizzle WE. Advanced concepts in fixation: 1. Effects of fixation on immunohistochemistry, reversibility of fixation and recovery of proteins, nucleic acids, and other molecules from fixed and processed tissues. 2. Developmental methods of fixation. J Histotechnol 2001;24;201-210.
- NTP. Report on carcinogens, Twelfth Edition. National Toxicology Program, USA Department of Health and Human Services, 2011; http://ntp.niehs.nih.gov/ntp/roc/twelfth/roc12.pdf November 7, 2011.
- NTP. Addendum to the 12th Report on Carcinogens. USA Department of Health and Human Services, National Toxicology Program, 2011; http://ntp.niehs.nih.gov/ntp/roc/twelfth/Addendum.pdf November 7, 2011.
- OSHA. Occupational Safety and Health Standards. Standard Number: 1910.1048 : Formaldehyde. United States Department of Labor, Occupational Safety and Health Administration, 2011; http://www.osha.gov/pls/oshaweb/owadisp.show_document?p_id=10075&p_table=STANDARDS November 7, 2011.
- Leica, Microsystems. Material Safety Data Sheet: 10% Millonig’s Buffered Formalin. 2007; http://www.leica-microsystems.com/index.php?id=1504&tx_leicaproducts_pi1[showUid]=3299&tx_leicaproducts_pi1[tab]=downloads&cHash=49baf1391ce5bcd25cd31e224782b369 27/10/2011.
- Bozzola JJ, Russell LD. Electron microscopy: principles and techniques for biologists. Boston: Jones and Bartlett, 1992.
Related Content
Die Inhalte des Knowledge Pathway von Leica Biosystems unterliegen den Nutzungsbedingungen der Website von Leica Biosystems, die hier eingesehen werden können: Rechtlicher Hinweis. Der Inhalt, einschließlich der Webinare, Schulungspräsentationen und ähnlicher Materialien, soll allgemeine Informationen zu bestimmten Themen liefern, die für medizinische Fachkräfte von Interesse sind. Er soll explizit nicht der medizinischen, behördlichen oder rechtlichen Beratung dienen und kann diese auch nicht ersetzen. Die Ansichten und Meinungen, die in Inhalten Dritter zum Ausdruck gebracht werden, spiegeln die persönlichen Auffassungen der Sprecher/Autoren wider und decken sich nicht notwendigerweise mit denen von Leica Biosystems, seinen Mitarbeitern oder Vertretern. Jegliche in den Inhalten enthaltene Links, die auf Quellen oder Inhalte Dritter verweisen, werden lediglich aus Gründen Ihrer Annehmlichkeit zur Verfügung gestellt.
Vor dem Gebrauch sollten die Produktinformationen, Beilagen und Bedienungsanleitungen der jeweiligen Medikamente und Geräte konsultiert werden.
Copyright © 2024 Leica Biosystems division of Leica Microsystems, Inc. and its Leica Biosystems affiliates. All rights reserved. LEICA and the Leica Logo are registered trademarks of Leica Microsystems IR GmbH.



